摘要:理解“位置.结构.性质 之间的辩证关系
网址:http://m.1010jiajiao.com/timu3_id_39763[举报]
(2011?宝鸡一模)化学选修3-物质结构与性质
元素X和Y属于同一主族.负二价的元素X和氢的化合物在通常情况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物M和N,在M和N中,Y的质量分数分别为50%和40%.
(1)与X、Y同主族且与Y相邻的Z元素在周期表中的位置为
(2)M化学式为
(3)写出与N互为等电子体的一种分子的化学式_
(4)由元素氢、X、Y三种元素形成的他合物常见的有两种.其水溶液均显酸性,试分别写出其分子式
查看习题详情和答案>>
元素X和Y属于同一主族.负二价的元素X和氢的化合物在通常情况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物M和N,在M和N中,Y的质量分数分别为50%和40%.
(1)与X、Y同主族且与Y相邻的Z元素在周期表中的位置为
第四周期ⅥA族
第四周期ⅥA族
,Z的基态原子删除此空
删除此空
的价层电子的排布式为4S24P4
4S24P4
.(2分)(2)M化学式为
SO2
SO2
;该分子是由极性
极性
键(填“极性”或“非极性”)形成的极性
极性
分子(填“极性”或“非极性”).(3)写出与N互为等电子体的一种分子的化学式_
BF3
BF3
;该分子中的中心原子以SP2
SP2
杂化,是非极性
非极性
分子(填“极性”或“非极性”),分子空间构型为平面三角形
平面三角形
.(4)由元素氢、X、Y三种元素形成的他合物常见的有两种.其水溶液均显酸性,试分别写出其分子式
H2SO4
H2SO4
、H2SO3
H2SO3
,并比较酸性强弱:H2SO4>H2SO3
H2SO4>H2SO3
.元素周期表不仅对元素进行了分类,也揭示了一系列的科学观念,如结构决定性质、量变引起质变、复杂现象中蕴涵着简洁的规律等,这对科学的发展等起到了积极的作用.下列说法中正确的是( )
查看习题详情和答案>>
 【化学--选修3:物质结构与性质】
【化学--选修3:物质结构与性质】已知X、Y和Z三种元素的原子序数之和等于48.X的一种1:2型氢化物分子中既有σ键又有π键,所有原子共平面.Z是金属元素,Z的单质和化合物有广泛的用途.已知Z的核电荷数小于28,且次外层有2个未成对电子.工业上利用ZO2和碳酸钡在熔融状态下制化合物M(M可看做一种含氧酸盐).经X射线分析,M晶体的最小重复单元为正方体(如图),顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.
(1)Y2+的结构示意图


3d24s2
3d24s2
.(2)X在该氢化物中以
sp2
sp2
方式杂化;X和Y形成的化合物YX2的电子式为

(3)①制备M的化学反应方程式是
TiO2+BaCO3
BaTiO3+CO2↑
| ||
TiO2+BaCO3
BaTiO3+CO2↑
;
| ||
②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-处于立方体的
面心
面心
;③已知O2-半径为1.4×10-10 m,Z4+的半径为6.15×10-11m,阿佛加德罗常数为NA,则M的密度为
| 233g/mol |
| (4.03×10-8 cm)3NA |
| 233g/mol |
| (4.03×10-8 cm)3NA |
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选择其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.
A:
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一.在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为 .
(2)写出基态Cu+的核外电子排布式 .
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为 .
(4)写出与CO互为等电子体的离子 .(任写一个)
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中 C原子轨道的杂化类型分别为 ;1mol尿素分子中,σ键的数目为 .
(6)铜金合金形成的晶胞如图1所示,其中Cu、Au原子个数比为 .
B:
对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到.
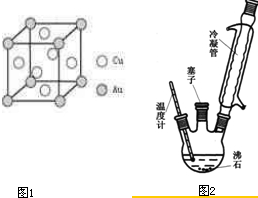
实验室可利用如图2实验装置合成对氨基苯磺酸.实验步骤如下:
1在一个250mL三颈烧瓶中加入10mL苯胺及几粒沸石,将三颈烧瓶放入冷水中冷却,小心地加入18mL浓硫酸.
2将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5h.
③将反应液冷却至约50℃后,倒入盛有100mL冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出,抽滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品.
④将粗产品用沸水溶解,冷却结晶(若溶液颜色过深,可用活性炭脱色),抽滤,收集产品,晾干.(说明:100mL水在20℃时可溶解对氨基苯磺酸1.08g,在100℃时可溶解6.67g.)
试回答填空.
(1)装置中冷凝管的作用是 .
(2)步骤②中采用油浴加热,下列说法正确的是 (填序号).
A.用油浴加热的好处是反应物受热均匀,便于控制温度
B.此处也可以改用水浴加热
C.实验装置中的温度计可以改变位置,也可使其水银球浸入在油中
(3)步骤③用少量冷水洗涤晶体的好处是 .
(4)步骤③和④均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先 ,然后 ,以防倒吸.
(5)步骤④中有时需要将“粗产品用沸水溶解,冷却结晶,抽滤”的操作进行多次,其目的是 .每次抽滤后均应将母液收集起来,进行适当处理,其目的是 .
查看习题详情和答案>>
A:
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一.在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为
(2)写出基态Cu+的核外电子排布式
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为
(4)写出与CO互为等电子体的离子
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中 C原子轨道的杂化类型分别为
(6)铜金合金形成的晶胞如图1所示,其中Cu、Au原子个数比为
B:
对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到.

实验室可利用如图2实验装置合成对氨基苯磺酸.实验步骤如下:
1在一个250mL三颈烧瓶中加入10mL苯胺及几粒沸石,将三颈烧瓶放入冷水中冷却,小心地加入18mL浓硫酸.
2将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5h.
③将反应液冷却至约50℃后,倒入盛有100mL冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出,抽滤,用少量冷水洗涤,得到的晶体是对氨基苯磺酸粗产品.
④将粗产品用沸水溶解,冷却结晶(若溶液颜色过深,可用活性炭脱色),抽滤,收集产品,晾干.(说明:100mL水在20℃时可溶解对氨基苯磺酸1.08g,在100℃时可溶解6.67g.)
试回答填空.
(1)装置中冷凝管的作用是
(2)步骤②中采用油浴加热,下列说法正确的是
A.用油浴加热的好处是反应物受热均匀,便于控制温度
B.此处也可以改用水浴加热
C.实验装置中的温度计可以改变位置,也可使其水银球浸入在油中
(3)步骤③用少量冷水洗涤晶体的好处是
(4)步骤③和④均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先
(5)步骤④中有时需要将“粗产品用沸水溶解,冷却结晶,抽滤”的操作进行多次,其目的是