摘要:2KClO32KCl + 3O2↑ 149 96 X 4.8 解得X=7.45g 所以.充分反应后,试管内含有KCl.MnO2两种物质,质量分别为7.45g和15-4.8-7.45=2.75g. 答:反应生成4.8克氧气,充分反应后,试管内含有KCl.MnO2两种物质,质量分别为7.45g和2.75g.14.(1)M=5g×5.0×106×110=2.75×109g, (2)M(煤)=4×103Kg×110=4.4×105Kg M(碳)= M(煤)×85%=4.4×105Kg×85%=3.74105Kg 设锅炉共可释放出X千克二氧化碳气体.则 C + O2 CO2 12 44
网址:http://m.1010jiajiao.com/timu3_id_3975337[举报]
下列化学方程式及基本反应类型均正确的是( )
A.氯酸钾制氧气 2KClO3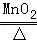 2KCl+3O2↑分解反应 2KCl+3O2↑分解反应 |
| B.含氢氧化铝的药物中和胃酸 2Al(OH)3+3H2SO4═Al2(SO4)3+6H20复分解反 |
| C.检验18K黄金 Cu+AgNO3═Ag+Cu(NO3)2置换反应 |
| D.高炉炼铁 Fe2O3+3CO═2Fe+3CO2置换反应 |
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用.
(1)为探究二氧化锰对氯酸钾分解的催化作用.在相同条件下,同学们按下表进行实验并记录相关数据.(其他影响实验的因素均相同)
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | ||
| 实验2 | a | MnO2 0.5 |
②表中的待测数据指______(填字母序号).
A.氧气的质量 B.反应后固体的质量 C.氧气的体积 D.单位时间内产生氧气的体积
③设计“实验1”的目的是______.
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应.氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3
 2KCl+3O2↑.已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空.
2KCl+3O2↑.已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空.(I)2KClO3+2MnO2
 2KMnO4+Cl2↑+O2↑;
2KMnO4+Cl2↑+O2↑;(II)______(用化学方程式表示);
(III)K2MnO4+Cl2
 2KCl+MnO2+O2↑.
2KCl+MnO2+O2↑.通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应.
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
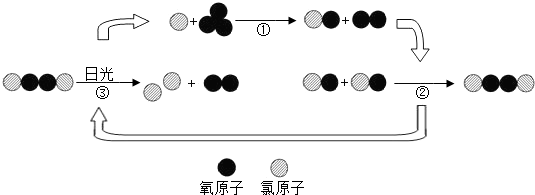
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式______. 查看习题详情和答案>>
小意和小思同学对化学计算很有心得.以下是他们解答一道计算题的实录.请你一起参与研究并完成相关问题.(计算结果精确到0.01)
[题目]已知:2KClO3 2KCl+3Q2↑,将10g氯酸钾和2g二氧化锰混合后放入试管中加热,收集所需量的氧气后,停止加热让试管冷却,称得试管内剩余固体的质量为7.2g.求生成氯化钾的质量.
2KCl+3Q2↑,将10g氯酸钾和2g二氧化锰混合后放入试管中加热,收集所需量的氧气后,停止加热让试管冷却,称得试管内剩余固体的质量为7.2g.求生成氯化钾的质量.
(1)小意很快得到(10g+2g-7.2g)是________(填化学式)的质量,进而求出KCl 的质量是________g.
(2)小思依据上述计算的结果发现题目数据有问题.请你通过简单的计算,论证他的发现.
查看习题详情和答案>>
下列化学方程式及基本反应类型均正确的是( )
|
| A. | 氯酸钾制氧气 2KClO3 |
|
| B. | 含氢氧化铝的药物中和胃酸 2Al(OH)3+3H2SO4═Al2(SO4)3+6H20 复分解反应 |
|
| C. | 检验18K黄金 Cu+AgNO3═Ag+Cu(NO3)2 置换反应 |
|
| D. | 高炉炼铁 Fe2O3+3CO═2Fe+3CO2 置换反应 |
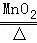 2KCl+3O2↑ 分解反应
2KCl+3O2↑ 分解反应