摘要:14. 某元素 的硫酸盐的式量是M, 硝酸盐的式量是N, 则该元素的化合价是 A. B. C. D.
网址:http://m.1010jiajiao.com/timu3_id_397479[举报]
在生产硫酸的钒废催化剂中,部分钒仍以V2O5形式存在,还有部分以VOSO4形式存在,约占总钒的30%~70%.工业上对废钒催化剂回收处理的工艺流程如下:
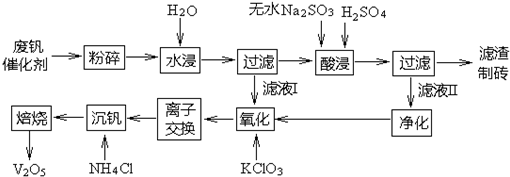
回答下列问题:
(1)“酸浸”是将钒废催化剂中V2O5转变成可溶于水的VOSO4(完全电离),请写出该反应的离子方程式______;酸浸液经分离净化后与水浸液合并,用氯酸钾氧化,使VOSO4氧化成可溶于水的(VO2)2SO4[(VO2)2SO4完全电离,氯元素被还原为Cl-],请写出该反应的离子方程式:______.
(2)加入适量的NH4Cl,钒以偏钒酸铵(NH4VO3)的形式沉淀析出.经过滤、焙烧可得到红棕色产品V2O5.在整个工业生产中没有涉及到的反应有______(填字母)
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
(3)在含有18.5gV2O5的样品中滴加60.00mL浓度为10.00mol?L-1HCl溶液,恰好完全反应(杂质不与盐酸反应),生成2.24L(标准状况)氯气,则生成物中V的化合价为______.
(4)上述滴加盐酸过程需要用滴定管,滴定管也常用于测定一定体积溶液中某溶质的含量,如果用蒸馏水洗涤滴定管后,就直接加入标准溶液进行滴定,则对滴定结果的影响是______.若锥形瓶用蒸馏水洗涤后,就直接装入待测溶液进行滴定,则对滴定结果的影响是______(以上填“偏高”、“偏低”或“无影响”).
查看习题详情和答案>>
在生产硫酸的钒废催化剂中,部分钒仍以V2O5形式存在,还有部分以VOSO4形式存在,约占总钒的30%~70%.工业上对废钒催化剂回收处理的工艺流程如下:

回答下列问题:
(1)“酸浸”是将钒废催化剂中V2O5转变成可溶于水的VOSO4(完全电离),请写出该反应的离子方程式______;酸浸液经分离净化后与水浸液合并,用氯酸钾氧化,使VOSO4氧化成可溶于水的(VO2)2SO4[(VO2)2SO4完全电离,氯元素被还原为Cl-],请写出该反应的离子方程式:______.
(2)加入适量的NH4Cl,钒以偏钒酸铵(NH4VO3)的形式沉淀析出.经过滤、焙烧可得到红棕色产品V2O5.在整个工业生产中没有涉及到的反应有______(填字母)
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
(3)在含有18.5gV2O5的样品中滴加60.00mL浓度为10.00mol?L-1HCl溶液,恰好完全反应(杂质不与盐酸反应),生成2.24L(标准状况)氯气,则生成物中V的化合价为______.
(4)上述滴加盐酸过程需要用滴定管,滴定管也常用于测定一定体积溶液中某溶质的含量,如果用蒸馏水洗涤滴定管后,就直接加入标准溶液进行滴定,则对滴定结果的影响是______.若锥形瓶用蒸馏水洗涤后,就直接装入待测溶液进行滴定,则对滴定结果的影响是______(以上填“偏高”、“偏低”或“无影响”).
查看习题详情和答案>>

回答下列问题:
(1)“酸浸”是将钒废催化剂中V2O5转变成可溶于水的VOSO4(完全电离),请写出该反应的离子方程式______;酸浸液经分离净化后与水浸液合并,用氯酸钾氧化,使VOSO4氧化成可溶于水的(VO2)2SO4[(VO2)2SO4完全电离,氯元素被还原为Cl-],请写出该反应的离子方程式:______.
(2)加入适量的NH4Cl,钒以偏钒酸铵(NH4VO3)的形式沉淀析出.经过滤、焙烧可得到红棕色产品V2O5.在整个工业生产中没有涉及到的反应有______(填字母)
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
(3)在含有18.5gV2O5的样品中滴加60.00mL浓度为10.00mol?L-1HCl溶液,恰好完全反应(杂质不与盐酸反应),生成2.24L(标准状况)氯气,则生成物中V的化合价为______.
(4)上述滴加盐酸过程需要用滴定管,滴定管也常用于测定一定体积溶液中某溶质的含量,如果用蒸馏水洗涤滴定管后,就直接加入标准溶液进行滴定,则对滴定结果的影响是______.若锥形瓶用蒸馏水洗涤后,就直接装入待测溶液进行滴定,则对滴定结果的影响是______(以上填“偏高”、“偏低”或“无影响”).
查看习题详情和答案>>
(2011?安庆三模)在生产硫酸的钒废催化剂中,部分钒仍以V2O5形式存在,还有部分以VOSO4形式存在,约占总钒的30%~70%.工业上对废钒催化剂回收处理的工艺流程如下:

回答下列问题:
(1)“酸浸”是将钒废催化剂中V2O5转变成可溶于水的VOSO4(完全电离),请写出该反应的离子方程式
(2)加入适量的NH4Cl,钒以偏钒酸铵(NH4VO3)的形式沉淀析出.经过滤、焙烧可得到红棕色产品V2O5.在整个工业生产中没有涉及到的反应有
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
(3)在含有18.5gV2O5的样品中滴加60.00mL浓度为10.00mol?L-1HCl溶液,恰好完全反应(杂质不与盐酸反应),生成2.24L(标准状况)氯气,则生成物中V的化合价为
(4)上述滴加盐酸过程需要用滴定管,滴定管也常用于测定一定体积溶液中某溶质的含量,如果用蒸馏水洗涤滴定管后,就直接加入标准溶液进行滴定,则对滴定结果的影响是
查看习题详情和答案>>

回答下列问题:
(1)“酸浸”是将钒废催化剂中V2O5转变成可溶于水的VOSO4(完全电离),请写出该反应的离子方程式
V2O5+SO32-+4H+=2VO2++SO42-+2H2O
V2O5+SO32-+4H+=2VO2++SO42-+2H2O
;酸浸液经分离净化后与水浸液合并,用氯酸钾氧化,使VOSO4氧化成可溶于水的(VO2)2SO4[(VO2)2SO4完全电离,氯元素被还原为Cl-],请写出该反应的离子方程式:C1O3-+6VO2++3H2O=6VO2++6H++C1-
C1O3-+6VO2++3H2O=6VO2++6H++C1-
.(2)加入适量的NH4Cl,钒以偏钒酸铵(NH4VO3)的形式沉淀析出.经过滤、焙烧可得到红棕色产品V2O5.在整个工业生产中没有涉及到的反应有
AD
AD
(填字母)A.化合反应 B.分解反应 C.复分解反应 D.置换反应
(3)在含有18.5gV2O5的样品中滴加60.00mL浓度为10.00mol?L-1HCl溶液,恰好完全反应(杂质不与盐酸反应),生成2.24L(标准状况)氯气,则生成物中V的化合价为
+4
+4
.(4)上述滴加盐酸过程需要用滴定管,滴定管也常用于测定一定体积溶液中某溶质的含量,如果用蒸馏水洗涤滴定管后,就直接加入标准溶液进行滴定,则对滴定结果的影响是
偏高
偏高
.若锥形瓶用蒸馏水洗涤后,就直接装入待测溶液进行滴定,则对滴定结果的影响是无影响
无影响
(以上填“偏高”、“偏低”或“无影响”).三草酸合铁(Ⅲ)酸钾晶体(K3[Fe(C2O4)3]?3H2O)有很重要的用途.可用如图流程来制备.根据题意完成下列各题:
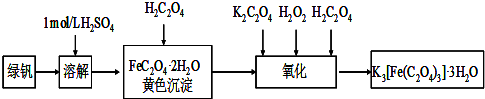
(1)若用铁和稀硫酸制备绿矾(FeSO4?7H2O)过程中,其中
(2)要从溶液中得到绿矾,必须进行的实验操作是
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
某兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?3H2O)中铁元素含量,做了如下实验:
步骤1:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液.
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO4-被还原成Mn2+.向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性.
步骤3:在酸性条件下,用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,共做三次实验,平均消耗KMnO4溶液20.00ml,滴定中MnO4-,被还原成Mn2+.
(3)步骤1中,配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有
(4)步骤2中,加入锌粉的目的是
(5)步骤3中,发生反应的离子方程式为:
(6)步骤2中,若加入的KMnO4的溶液的量不够,则测得的铁含量
(7)某同学将8.74g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647g/L(已折合成标准状况下)气体.研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3.写出该分解反应的化学方程式
查看习题详情和答案>>

(1)若用铁和稀硫酸制备绿矾(FeSO4?7H2O)过程中,其中
铁
铁
(填物质名称)往往要过量,理由是防止Fe2+被氧化
防止Fe2+被氧化
.(2)要从溶液中得到绿矾,必须进行的实验操作是
bcae
bcae
.(按前后顺序填)a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
某兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?3H2O)中铁元素含量,做了如下实验:
步骤1:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液.
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO4-被还原成Mn2+.向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性.
步骤3:在酸性条件下,用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,共做三次实验,平均消耗KMnO4溶液20.00ml,滴定中MnO4-,被还原成Mn2+.
(3)步骤1中,配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有
250ml容量瓶
250ml容量瓶
;主要操作步骤依次是:称量、溶解、转移、洗涤
洗涤
、定容、摇匀.(4)步骤2中,加入锌粉的目的是
还原Fe3+为Fe2+
还原Fe3+为Fe2+
.(5)步骤3中,发生反应的离子方程式为:
MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O
MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O
.(6)步骤2中,若加入的KMnO4的溶液的量不够,则测得的铁含量
偏高
偏高
.(选填“偏低”、“偏高”、“不变”)(7)某同学将8.74g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647g/L(已折合成标准状况下)气体.研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3.写出该分解反应的化学方程式
2K3[Fe(C2O4)3]═3K2CO3+Fe+FeO+4CO+5CO2
2K3[Fe(C2O4)3]═3K2CO3+Fe+FeO+4CO+5CO2
.(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
① 写出制取高铁酸钠的化学方程式: ;
② 在制取高铁酸钠的反应中 元素被氧化;
③ 高铁酸钠杀菌作用是利用了其具有的 ,而净水作用的原因是 。
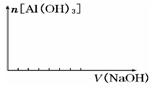
(2)在某化工厂生产中,要用到一种无色、可溶于水的晶体铝铵矾。该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵。向该复盐的溶液中逐滴加入氢氧化钠溶液,将发生一系列变化。已知,NH4+与AlO2-在水溶液中不能大量共存,会发生如下反应:NH4++A1O2-+H2O=Al(OH)3↓+ NH3↑ ,试回答:
① 硫酸铝铵在水溶液中的电离方程式为 ;
② 在向该复盐的溶液中逐滴加入氢氧化钠溶液,请在下图中画出加入氢氧化钠溶液的体积与沉淀物质的量之间的关系。