网址:http://m.1010jiajiao.com/timu3_id_397472[举报]
某同学旅游时发现,苗族人的银饰美丽而富有民族文化,制作银饰时可以选 用Fe(NO3)3溶液做蚀刻剂。受此启发,该同学所在的化学兴趣小组在实验室选用Fe(NO3)3 溶液清洗做过银镜反应的试管,发现不但银镜溶解,而且较少产生刺激性气体。
化学兴趣小组对Fe(NO3)3溶液溶解银的原理进行探究:
【提出假设】假设1: Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化Ag;
假设2:Fe3+具有氧化性,能氧化Ag
【验证假设】
(1)甲同学验证假设1。
①他用淡紫色的Fe(N03)3·9H20晶体(分析纯,Mr=404)配制1.5mol/L的Fe(N03)3 落液100mL。需要称取_____g Fe(N03)3·9H20晶体,配制过程中所用到的仪器除烧杯、 玻璃棒外还必需:__________
②测得1.5 mol/L的Fe(NO3)3溶液pH约为1,其原因用化学用语表示为____。
③将pH=1的HN03溶液加入到镀有银镜的试管中,振荡,观察到银镜慢慢溶解,产生 无色气体并在液面上方变为红棕色,溶液中发生反应的离子方程式应是_____
④将1.5mol/L的Fe(NO3)3溶液加入到镀有银镜的试管中,振荡,观察到银镜很快溶解, 并且溶液颜色加深。
(2)乙同学验证假设2。分别用溶质的质量分数为2%、10%的足量FeCl3溶液加入到镀 有银镜的试管中,振荡,都看不出银镜溶解。乙同学由此得出结论,假设2不成立。
你是否同意乙的结论?_______,简述理由:_______
【思考与交流】I甲同学的实验④中,溶液颜色为什么会加深?查阅资料得知,Fe2+能与 NO形成配离子: (棕色)。已知,同浓度的硝酸氧化性比Fe3+略强。
(棕色)。已知,同浓度的硝酸氧化性比Fe3+略强。
根据以上信息综合分析,浓、稀Fe(N03)3溶液溶解银镜时,发生的反应有何不同?
__________________________________________
查看习题详情和答案>>
某同学进行实验研究时,欲配制1.0 mol·L-1 Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量∶315).在室温下配制溶液时发现所取试剂在足量的水中仅部分溶解,烧杯中存在大量未溶物.为探究原因,该同学查得Ba(OH)2·8H2O在283 K、293 K和303 K时的溶解度(g/100 g H2O)分别为2.5、3.9和5.6.
1.烧杯中未溶物可能仅为BaCO3,理由是________.
2.假设试剂由大量Ba(OH)2·8H2O和少量BaCO3组成,设计实验方案,进行成分检验.在答题纸上进一步完成实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器∶稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管

将试剂初步提纯后,准确测定其中Ba(OH)2·8H2O的含量.实验如下∶
3.配制250 ml约0.1 mol·L-1 Ba(OH)2溶液∶准确称取w克试样,置于烧杯中,加适量蒸馏水,________,将溶液转入________,洗涤,定容,摇匀.
4.滴定∶准确量取25.00 ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将________(填“0.020”、“0.05”、“0.1980”或“1.5”)mol·L-1盐酸装入50 ml酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸Vml.计算Ba(OH)2·8H2O的质量分数=________(只列出算式,不做运算)
5.室温下,________(填“能”或“不能”)配制1.0 mol·L-1 Ba(OH)2溶液.
已知某亚铁盐的化学式可表示为(NH4)a Feb(s04)c。取一定质量的该亚铁盐样品全部溶于足量的水中,将所得溶液平均分为两份。一份溶液中加入足量的BaCl2溶液,得到白色沉淀9.32 g。另一份溶液同足量的浓NaOH溶液共热,产生的氨气用100 mL 0.5mo1·L-1稀硫酸吸收后(设产生的氨全部逸出),剩余的硫酸再用1.5 mol·L-1NaOH溶液中和,需NaOH溶液40mL。该亚铁盐样品中b:c的比值为
A.1:1 B.2:1 C.1:2 D.3:2
查看习题详情和答案>>
(18分)电子工业常用30﹪的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,应考虑回收利用。按如下流程在实验室进行实验:从废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。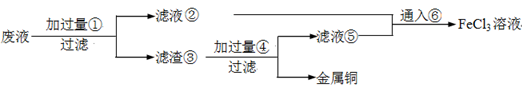
(1)写出FeCl3溶液与铜箔发生反应的化学方程式: 。
(2)检验废腐蚀液中含有Fe3+的实验操作是
(3)“过滤”用到的玻璃仪器有:普通漏斗、 。
(4)废液中加入过量①后,发生反应的离子方程式:
(5)上述流程中取废液200 mL,其中含CuCl2 1.5 mol·L—1、FeCl2 3.0 mol·L—1、FeCl3 1.0 mol·L—1,若要将铜全部回收,需加入Fe粉的质量应不少于_____________g;将铁的化合物全部转化为FeCl3溶液需通入Cl2的物质的量不少于_______________mol。
(6)某化学兴趣小组利用在下图装置制取氯气并通入到FeCl2溶液中获得FeCl3溶液。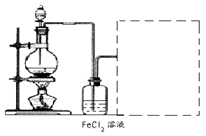
制备Cl2的化学方程式为:
该装置不完整,请在所给虚线框内画出所缺部分,并标注试剂。
(10分)
现用质量分数为36.5%、密度为1.20 g·cm-3的浓盐酸来配制100 mL 1.5 mol/L的稀盐酸。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒⑥容量瓶 ⑦托盘天平 ⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀盐酸时用不到的有 (填代号)。
(2)经计算,需浓盐酸的体积为 。
现有①10 mL ②20 mL ③50 mL ④100 mL四种规格的量筒,取用浓盐酸应选用的量筒是 (填代号)。
(3)在配制过程中,其他操作都准确,下列操作中:错误的是 ,能引起误差偏高的有 (填序号)。
①洗涤量取浓盐酸后的量筒,并将洗涤液转移到容量瓶中
②稀释后的盐酸在空气中放置过久
③定容时,加蒸馏水超过标线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑥定容时,俯视标线
查看习题详情和答案>>