摘要:在H2SO4中氢.硫.氧三种元素的质量比的计算式正确的是 A. B.1:32:16 C.2:1:4 D. ☆三.计算化合物中某元素的质量分数 某元素的相对原子质量×原子个数 某元素的质量分数 = ×100% 化合物的相对分子质量 例题:计算碳酸氢铵[NH4HCO3]中氮元素的质量分数: N 解: NH4HCO3 中氮元素的质量分数 N%=的子分子质量 ×100%= 14 ×100%=17.7% NH4HCO3 79 练习:计算化肥尿素[CO(NH2)2]中氮元素的质量分数.
网址:http://m.1010jiajiao.com/timu3_id_3971749[举报]
在硫酸(H2SO4)中,氢、硫、氧三种元素的质量比为________;98g硫酸中,氢元素的质量为________g;在________g硫酸中含氢元素的质量跟36g水中含氢元素的质量相同.
查看习题详情和答案>>26、空气是一种十分重要的天然资源.
(1)空气成分按体积计算,含量最多的是
(2)实验室可通过多种途径制取氧气,如分解过氧化氢、加热高锰酸钾、电解水等,因为这三种物质都含有
(3)保护空气,提倡“低碳”,减少温室效应,是我们必须关注的问题.科学家正在研究如图所示的二氧化碳新的循环体系.

从图中分析得出的下列结论中,正确的是
A.二氧化碳也是一种重要的资源 B.利用降温、加压将二氧化碳分离是化学变化
C.二氧化碳与氢气在复合催化剂下反应产物是混合物 D.液化石油气、汽油、甲醇等物质燃烧都有二氧化碳产生
(4)酸雨的形成主要是二氧化硫与水作用产生的亚硫酸(H2SO3)被空气中的氧气氧化为硫酸(H2SO4)的缘故.该氧化反应的化学方程式为
(5)“绿色化学”的特点之一是“零排放”.一定条件下,一氧化碳和氢气可以按照不同比例反应,若只生成一种产物就能实现“零排放”,符合这一要求的产物是
A.甲醇(CH4O) B.甲醛(CH2O)
C.乙醇(C2H6O) D.乙醛(C2H4O)
查看习题详情和答案>>
(1)空气成分按体积计算,含量最多的是
N2
(填写化学式).(2)实验室可通过多种途径制取氧气,如分解过氧化氢、加热高锰酸钾、电解水等,因为这三种物质都含有
O
元素(填元素符号);从降低能量消耗上思考,你选择的实验室制取氧气的方法是分解过氧化氢
.(3)保护空气,提倡“低碳”,减少温室效应,是我们必须关注的问题.科学家正在研究如图所示的二氧化碳新的循环体系.

从图中分析得出的下列结论中,正确的是
ACD
(填字母序号).A.二氧化碳也是一种重要的资源 B.利用降温、加压将二氧化碳分离是化学变化
C.二氧化碳与氢气在复合催化剂下反应产物是混合物 D.液化石油气、汽油、甲醇等物质燃烧都有二氧化碳产生
(4)酸雨的形成主要是二氧化硫与水作用产生的亚硫酸(H2SO3)被空气中的氧气氧化为硫酸(H2SO4)的缘故.该氧化反应的化学方程式为
SO2+H2O═H2SO3;2H2SO3+O2═2H2SO4
(5)“绿色化学”的特点之一是“零排放”.一定条件下,一氧化碳和氢气可以按照不同比例反应,若只生成一种产物就能实现“零排放”,符合这一要求的产物是
A、B
(填字母序号).A.甲醇(CH4O) B.甲醛(CH2O)
C.乙醇(C2H6O) D.乙醛(C2H4O)
(2013?海淀区二模)下列A~G七种物质由氢、碳、氧、钠、硫、钙中的两种或三种元素组成.
(1)A、B、C都是氧化物.A与B反应的产物可以使紫色石蕊溶液变成红色.B与C化合后的产物D可以使无色酚酞溶液变红,则B的化学式是
(2)E是一种常见的液体燃料,在汽油中加入适量的E可以作为汽车燃料.E在氧气中燃烧可生成A和B,则E燃烧的化学方程式为
(3)F在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产,F与G反应的生成物中有A,则F的俗称是
(4)D可中和某些工厂污水中含有的G,D与G反应的化学方程式为
(5)D与F固体混合物溶于水后发生化学反应,写出所得溶液中溶质的所有可能组成:
查看习题详情和答案>>
(1)A、B、C都是氧化物.A与B反应的产物可以使紫色石蕊溶液变成红色.B与C化合后的产物D可以使无色酚酞溶液变红,则B的化学式是
CO2
CO2
.(2)E是一种常见的液体燃料,在汽油中加入适量的E可以作为汽车燃料.E在氧气中燃烧可生成A和B,则E燃烧的化学方程式为
C2H6O+3O2
2CO2+3H2O
| ||
C2H6O+3O2
2CO2+3H2O
.
| ||
(3)F在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产,F与G反应的生成物中有A,则F的俗称是
纯碱
纯碱
,F与G反应的化学方程式是Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
;(4)D可中和某些工厂污水中含有的G,D与G反应的化学方程式为
Ca(OH)2+H2SO4=CaSO4+2H2O
Ca(OH)2+H2SO4=CaSO4+2H2O
.(5)D与F固体混合物溶于水后发生化学反应,写出所得溶液中溶质的所有可能组成:
NaOH,NaOH、Ca(OH)2,NaOH、Na2CO3
NaOH,NaOH、Ca(OH)2,NaOH、Na2CO3
(填化学式).草酸(H2C2O4)晶体在浓H2SO4存在时,加热分解为A、B、C三种初中常见的氧化物.其中C为最常见的溶剂,组成A、B两物质的元素相同,组成草酸和D物质的元素也相同.各物质之间的关系如图所示(反应条件已省略).
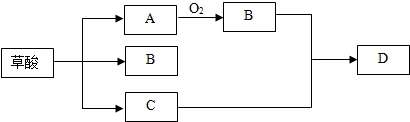
根据以上信息回答下列问题:
(1)草酸的化学式量为:
(2)A物质的化学式为
(3)B+C→D的化学方程式为:
(4)草酸在浓硫酸催化作用下热分解的化学方程式为
查看习题详情和答案>>

根据以上信息回答下列问题:
(1)草酸的化学式量为:
90
90
,其中碳、氢、氧元素的质量比为12:1:32
12:1:32
.(2)A物质的化学式为
CO
CO
;(3)B+C→D的化学方程式为:
CO2+H2O=H2CO3
CO2+H2O=H2CO3
;(4)草酸在浓硫酸催化作用下热分解的化学方程式为
H2C2O4
CO↑+CO2↑+H2O
| ||
| △ |
H2C2O4
CO↑+CO2↑+H2O
.
| ||
| △ |