摘要:4.氯酸钾和二氧化锰组成的混合物15.5g装入试管中.加热制取氧气.待反应完全后.将试管冷却.称量.得到10.7g固体物质.计算: 10.7g固体物质中含有哪些物质?各多少克?
网址:http://m.1010jiajiao.com/timu3_id_3969998[举报]
下图所示的是实验室常用的实验装置.
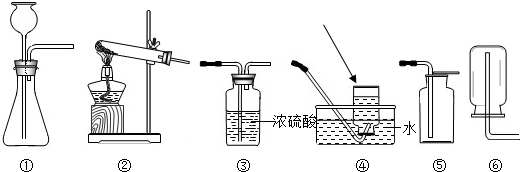
(1)图中所示仪器中,箭头所示名称为 .
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起 作用,反应的化学反应式为 .其发生装置为 (填序号,下同),收集装置可以选取 .
(3)此实验包括以下操作:①加热;②收集气体;③检查气密性;④装入高锰酸钾;
⑤将导管从水中移出;⑥熄灭酒精灯.正确的操作顺序是 (填序号)
(4)如果选用过氧化氢和二氧化锰制取氧气,优点是 ;
A生成物只有氧气;B不需要加热;C需要加热;D原料易得
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
问题:从上表中能得出哪些结论?(只任写一条)如实验室用过氧化氢和二氧化锰的混合物制氧气,请写出反应式 .
(6)如何证明制取的气体是否为氧气? 查看习题详情和答案>>

(1)图中所示仪器中,箭头所示名称为
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起
(3)此实验包括以下操作:①加热;②收集气体;③检查气密性;④装入高锰酸钾;
⑤将导管从水中移出;⑥熄灭酒精灯.正确的操作顺序是
(4)如果选用过氧化氢和二氧化锰制取氧气,优点是
A生成物只有氧气;B不需要加热;C需要加热;D原料易得
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
| 浓度 时间(min) 条件 |
30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
(6)如何证明制取的气体是否为氧气? 查看习题详情和答案>>
下图所示的是实验室常用的实验装置.
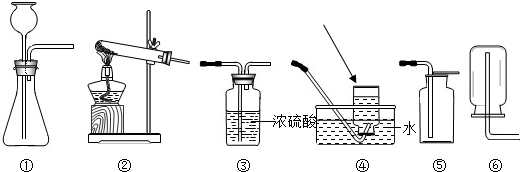
(1)图中所示仪器中,箭头所示名称为______.
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起______作用,反应的化学反应式为______.其发生装置为______(填序号,下同),收集装置可以选取______.
(3)此实验包括以下操作:①加热;②收集气体;③检查气密性;④装入高锰酸钾;
⑤将导管从水中移出;⑥熄灭酒精灯.正确的操作顺序是______(填序号)
(4)如果选用过氧化氢和二氧化锰制取氧气,优点是______;
A生成物只有氧气;B不需要加热;C需要加热;D原料易得
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
问题:从上表中能得出哪些结论?(只任写一条)如实验室用过氧化氢和二氧化锰的混合物制氧气,请写出反应式______.
(6)如何证明制取的气体是否为氧气?
查看习题详情和答案>>

(1)图中所示仪器中,箭头所示名称为______.
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起______作用,反应的化学反应式为______.其发生装置为______(填序号,下同),收集装置可以选取______.
(3)此实验包括以下操作:①加热;②收集气体;③检查气密性;④装入高锰酸钾;
⑤将导管从水中移出;⑥熄灭酒精灯.正确的操作顺序是______(填序号)
(4)如果选用过氧化氢和二氧化锰制取氧气,优点是______;
A生成物只有氧气;B不需要加热;C需要加热;D原料易得
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
| 浓度 时间(min) 条件 |
30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
(6)如何证明制取的气体是否为氧气?
某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空.
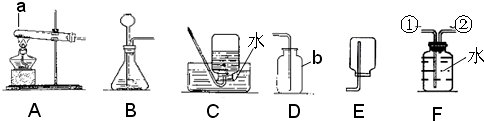
(1)写出图中仪器a、b的名称 a________,b________.
(2)实验室制取二氧化碳的化学方程式是________.应选择的气体发生装置是________,气体收集装置是________.
(3)实验室加热高锰酸钾制取氧气的化学方程式是________,应选择的发生装置是________,若用盛满水的F装置收集氧气,应从导管________(填①或②)通入.
(4)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是________.
(5)取氯酸钾和二氧化锰的混合物15.5克,放入一大试管中加热,反应完全后冷却到反应前温度,称残余固体质量为10.7克.求生成氧气多少克?生成氯化钾多少克?
查看习题详情和答案>>
某化学兴趣小组回收利用废旧干电池.
【实验1】回收填料中的二氧化锰和氯化铵
【查阅资料】废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如下图所示.

(1)操作1的名称是 ,该操作中玻璃棒的作用是 .
(2)灼烧滤渣l的目的是 .
(3)二氧化锰是氯酸钾受热分解的催化剂,下表是他们的有关实验数据,请你回答有关问题:
①据上表可知二氧化锰与氯酸钾的质量比为 时,反应速率最快.分析可知反应前后二氧化锰在固体混合物中质量分数是 (“不变”或“变大”或“变小”).
②二氧化锰的用量过少时产生氧气的速率很慢,原因是 ;二氧化锰用量过多,产生氧气的速率 (填“变快”、“变慢”或“不变”),通过分析可知,在化学反应中催化剂的用量 (填“是”或“不是”)越多越好.
【实验2】利用外壳回收物锌制取氢气及相关探究
(4)用锌粒和稀硫酸可制取氢气(锌+硫酸→硫酸锌+氢气).己知氢气密度比空气小且难溶于水,提供装置如下图:应选择:发生装置为 (填编号),排空气法收集装置为 (填编号).
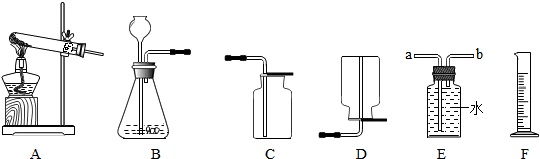
(5)探究影响锌与稀硫酸反应快慢的因素.反应过程中,用前10min内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如下表.
①比较实验a和实验b,可以得到的结论是 .
②为了研究硫酸浓度对反应快慢的影响,需比较实验 和实验 (填编号).
③控制其他条件相同,需控制的条件是 (例举一种条件即可).
查看习题详情和答案>>
【实验1】回收填料中的二氧化锰和氯化铵
【查阅资料】废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如下图所示.

(1)操作1的名称是
(2)灼烧滤渣l的目的是
(3)二氧化锰是氯酸钾受热分解的催化剂,下表是他们的有关实验数据,请你回答有关问题:
| 二氧化锰与氯酸钾的质量比 |
|
|
|
|
|
|
|
|
| ||||||||||||||||||
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
②二氧化锰的用量过少时产生氧气的速率很慢,原因是
【实验2】利用外壳回收物锌制取氢气及相关探究
(4)用锌粒和稀硫酸可制取氢气(锌+硫酸→硫酸锌+氢气).己知氢气密度比空气小且难溶于水,提供装置如下图:应选择:发生装置为

(5)探究影响锌与稀硫酸反应快慢的因素.反应过程中,用前10min内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如下表.
| 验实 号编 |
试剂 | 前 10min 内产生 的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30mL 30% | 564.3 |
| b | 含杂质的锌 | 30mL 30% | 634.7 |
| c | 纯锌 | 30mL 20% | 449.3 |
| d | 纯锌 | 40mL 30% | 602.8 |
②为了研究硫酸浓度对反应快慢的影响,需比较实验
③控制其他条件相同,需控制的条件是