网址:http://m.1010jiajiao.com/timu3_id_396376[举报]
①氧化钠、②氢氧化钠、③过氧化钠、④亚硫酸钠。各1mol上述固体物质,长期放置于空气中,最后质量增加情况是(不考虑潮解因素)
A. ①=②>③>④ B. ①>③>④>②
C. ②>①=③>④ D. ④>②>③>①
查看习题详情和答案>>I、(10分)过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~F涉及H2O2的反应,回答相关问题:
A.2 H2O2=2 H2O+O2↑ B.Na2O2 +2HCl= 2NaCl+H2O2
C.Ag2O+ H2O2=2Ag+O2↑+ H2O
D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O
E.H2O2+MnSO4 = MnO2 + H2SO4 F.H2O2 +2Fe2++2H+== 2Fe3++2H2O
(1)上述反应不属于氧化还原反应的是(填代号)_____________。
(2)H2O2仅体现还原性的反应是(填代号) 。
(3)H2O2既体现氧化性又体现还原性的反应是(填代号) 。
(4)通过以上反应分析,H2O2常称为绿色氧化剂,原因是___________________
(5)上述反应说明H2O2、Ag2O、MnO2氧化性由强到弱的顺序是:
II、(6分)某实验小组为探究ClO-、I2、SO![]() 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠(NaClO)溶液,并加入少量的稀硫酸,只发现溶液立即变蓝;(已知I2遇淀粉变蓝)
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠(NaClO)溶液,并加入少量的稀硫酸,只发现溶液立即变蓝;(已知I2遇淀粉变蓝)
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠(Na2SO3)溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式
(2)实验②的化学反应中转移电子的物质的量是____________。
(3)以上实验说明,在酸性条件下ClO-、I2、SO![]() 的氧化性由弱到强的顺序是________。
的氧化性由弱到强的顺序是________。
氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等。为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
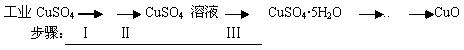
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀pH |
6.0 |
7.5 |
1.4 |
|
沉淀完全pH |
13 |
14 |
3.7 |
⑴ 步骤Ⅰ的目的是除不溶性杂质。所需操作的名称是________、________。
⑵ 步骤Ⅱ的目的是除硫酸亚铁。操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。
①写出用H2O2溶液除去硫酸亚铁的离子方程式____________________________。
②调整pH 的范围应该在____________之间。
⑶ 步骤Ⅲ的目的是得到CuSO4·5H2O晶体。操作是将溶液加热蒸发至有晶膜出现时,停止加热,_____________,水浴加热烘干。采用水浴加热的原因是____ 。
⑷ 该同学用CuSO4溶液进行如下探究实验:取A、B两支试管,分别加入 2 mL 5%H2O2溶液,再向H2O2溶液中分别滴入0.1 mol·L-1 FeCl3和CuSO4溶液各1 mL,摇匀,观察到滴入FeCl3 溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确________(填正确或错误),请说明原因 。
(5)16克硫酸铜固体投入水中形成1升溶液,则该溶液显 性(填“酸性”或“碱性”或“中性”),溶液中所有阳离子总数 0.1NA(填“等于”或“大于”或“小于”),若在上述新配制溶液加入稀硫酸再加入铁片产生氢气速率会明显加快,原因是 ;室温下、若在上述新配制溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时c(Cu2+)=________________mol·L-1(Kap[Cu(OH)2]=2.2×10-20)。
查看习题详情和答案>>
(4分)钠、铁两种金属单质及其化合物在生产、生活中有着广泛的应用。请回答:
(1)两种金属中,最高价氧化物的水化物属于强碱的是____,由此说明,钠的金属性比铁____(填“强”或“弱”)。
(2)某些补铁剂的成分是硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是____(填序号)。
① 稀盐酸 ② 石蕊溶液 ③ KSCN溶液
(3)向硫酸亚铁溶液中滴入氢氧化钠溶液,生成的灰白色沉淀迅速变成灰绿色,最后变成红褐色,此过程中涉及的氧化还原反应的化学方程式为
查看习题详情和答案>>
(1)Na2O2、K2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最合适的过氧化物是___________。
(2)过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:_________________________________________。
(3)与过氧化氢具有相同电子总数且属于非极性分子的有___________、___________(举两例,写化学式)。
(4)纯的过氧化氢常用作火箭燃料的氧化剂,已知0.4mol液态肼(N2H4)与足量的液态过氧化氢反应,生成N2和H2O(g),放出256.6kJ的热量。则该反应的热化学方程式为_______________________________________________。
查看习题详情和答案>>