摘要:2.写出下列物质的化学式及式量: (1)氧化铁 . (2)硫酸钠 . (3)氧化钠 . (4)碳酸钾 . (5)氢氧化钠 . (6)氯化钡 .
网址:http://m.1010jiajiao.com/timu3_id_3961724[举报]
同学们在用某硫酸溶液处理金属废料(主要是生铁)时,观察到溶液发烫并闻到刺激性气味,这种反常现象引起同学们的思考.从元素组成的角度分析,他们猜测气体可能是SO2、CO、CO2、H2中的一种或几种.

(1)甲同学认为废气中一定有SO2,原因是
(2)为了确定该气体的成分,同学们设计了一套合理的实验装置,如下图所示(铁架台已略去).请你从下列试剂中选择药品并结合实验装置完成实验.
药品:澄清石灰水,酸性高锰酸钾溶液,无水硫酸铜(遇水变蓝),碱石灰(吸收水和CO2). (药品可重复选用,每一步均反应充分)

(Ⅰ)B中盛放的试剂是
(Ⅱ)若观察到
(Ⅲ)D中反应前有样品10g(样品中可能混有铁),完全反应后剩余固体7.6g,则原样品的成分为:
查看习题详情和答案>>

(1)甲同学认为废气中一定有SO2,原因是
上述气体中只有SO2有刺激性气味
上述气体中只有SO2有刺激性气味
.(2)为了确定该气体的成分,同学们设计了一套合理的实验装置,如下图所示(铁架台已略去).请你从下列试剂中选择药品并结合实验装置完成实验.
药品:澄清石灰水,酸性高锰酸钾溶液,无水硫酸铜(遇水变蓝),碱石灰(吸收水和CO2). (药品可重复选用,每一步均反应充分)

(Ⅰ)B中盛放的试剂是
澄清石灰水
澄清石灰水
,A、B装置不能互换,原因是:SO2也能使澄清石灰水变浑浊,无法判断是否含有CO2
SO2也能使澄清石灰水变浑浊,无法判断是否含有CO2
.(Ⅱ)若观察到
D中的固体由红变黑,E中无明显变化,F中澄清石灰水变浑浊;
D中的固体由红变黑,E中无明显变化,F中澄清石灰水变浑浊;
现象,证明原气体中有CO无H2.写出D中反应的化学方程式3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(Ⅲ)D中反应前有样品10g(样品中可能混有铁),完全反应后剩余固体7.6g,则原样品的成分为:
氧化铁:8g 铁:2g;
氧化铁:8g 铁:2g;
.(写出物质及其对应的质量)某学习小组对硫酸进行如下研究:
(1)已知相同温度下,硫酸的质量分数越大溶液的酸性越强.若对稀硫酸进行如下操作,溶液的pH因化学变化而升高的有________(填字母).
A.加少量水 B.加少量铁粉 C.加少量氢氧化钾 D.加少量浓硫酸
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
①若量取硫酸甲时俯视读数,则所配硫酸乙的溶质质量分数将________(填填“偏大”、“偏小”或“不变”.
②由表中实验数据可知:有关硫酸吸水性的说法不正确的是________(填字母).
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强
(3)在高效复习课堂中,同学们利用稀释后的稀硫酸,硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中符合下列条件的两个化学方程式:一个中和反应________;一个有沉淀生成的反应________.
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.经测定,该溶液显酸性.则在该溶液中一定含有的离子是________.为了验证该溶液中可能含有的阴离子是否存在,请按如下实验进行验证.
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
| ________ | ________ |
某学习小组对硫酸进行如下研究:
(1)已知相同温度下,硫酸的质量分数越大溶液的酸性越强.若对稀硫酸进行如下操作,溶液的pH因化学变化而升高的有 (填字母).
A.加少量水 B.加少量铁粉 C.加少量氢氧化钾 D.加少量浓硫酸
(2)向两个烧杯中分别注入硫酸甲(溶质质量分数为98%,密度为1.84g/cm3)和硫酸乙(硫酸甲与水的按体积比1:1混和)各10mL,称量并记录不同时间(h)两种硫酸溶液吸水的质量,数据见下表:
①若量取硫酸甲时俯视读数,则所配硫酸乙的溶质质量分数将 (填填“偏大”、“偏小”或“不变”.
②由表中实验数据可知:有关硫酸吸水性的说法不正确的是 (填字母).
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强
(3)在高效复习课堂中,同学们利用稀释后的稀硫酸,硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中符合下列条件的两个化学方程式:一个中和反应 ;一个有沉淀生成的反应 .
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.经测定,该溶液显酸性.则在该溶液中一定含有的离子是 .为了验证该溶液中可能含有的阴离子是否存在,请按如下实验进行验证.
查看习题详情和答案>>
(1)已知相同温度下,硫酸的质量分数越大溶液的酸性越强.若对稀硫酸进行如下操作,溶液的pH因化学变化而升高的有 (填字母).
A.加少量水 B.加少量铁粉 C.加少量氢氧化钾 D.加少量浓硫酸
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
①若量取硫酸甲时俯视读数,则所配硫酸乙的溶质质量分数将 (填填“偏大”、“偏小”或“不变”.
②由表中实验数据可知:有关硫酸吸水性的说法不正确的是 (填字母).
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强
(3)在高效复习课堂中,同学们利用稀释后的稀硫酸,硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中符合下列条件的两个化学方程式:一个中和反应 ;一个有沉淀生成的反应 .
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.经测定,该溶液显酸性.则在该溶液中一定含有的离子是 .为了验证该溶液中可能含有的阴离子是否存在,请按如下实验进行验证.
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
(9分)某学习小组对硫酸进行如下研究:
(1)已知相同温度下,硫酸的质量分数越大溶液的酸性越强。若对稀硫酸进行如下操作,溶液的pH因化学变化而升高的有 (填字母)。
A.加少量水 B.加少量铁粉 C.加少量氢氧化钾 D.加少量浓硫酸
(2)向两个烧杯中分别注入硫酸甲(溶质质量分数为98%,密度为1.84g/cm3)和硫酸乙(硫酸甲与水的按体积比1︰1混和)各10mL,称量并记录不同时间(h)两种硫酸溶液吸水的质量,数据见下表:
①若量取硫酸甲时俯视读数,则所配硫酸乙的溶质质量分数将 (填填“偏大”、“偏小”或“不变”。
②由表中实验数据可知:有关硫酸吸水性的说法不正确的是 (填字母)。
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强(3)在高效复习课堂中,同学们利用稀释后的稀硫酸,硝酸钡、氢氧化钠、碳酸钾等物质的溶液对 “复分解反应发生的条件”进行再探究。
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中符合下列条件的两个化学方程式:
一个中和反应 ;一个有沉淀生成的反应 。
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液。经测定,该溶液显酸性。则在该溶液中一定含有的离子是 。为了验证该溶液中可能含有的阴离子是否存在,请按如下实验进行验证。
(1)已知相同温度下,硫酸的质量分数越大溶液的酸性越强。若对稀硫酸进行如下操作,溶液的pH因化学变化而升高的有 (填字母)。
A.加少量水 B.加少量铁粉 C.加少量氢氧化钾 D.加少量浓硫酸
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
①若量取硫酸甲时俯视读数,则所配硫酸乙的溶质质量分数将 (填填“偏大”、“偏小”或“不变”。
②由表中实验数据可知:有关硫酸吸水性的说法不正确的是 (填字母)。
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强(3)在高效复习课堂中,同学们利用稀释后的稀硫酸,硝酸钡、氢氧化钠、碳酸钾等物质的溶液对 “复分解反应发生的条件”进行再探究。
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中符合下列条件的两个化学方程式:
一个中和反应 ;一个有沉淀生成的反应 。
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液。经测定,该溶液显酸性。则在该溶液中一定含有的离子是 。为了验证该溶液中可能含有的阴离子是否存在,请按如下实验进行验证。
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
| | |
 小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题:
小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题:
(1)电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是______.
(2)经过溶液的学习后,小华明白了不是所有的溶液都能导电的道理,下列物质加入水中充分振荡后能导电的是______.
A.蔗糖 B.植物油 C.高锰酸钾 D.碳酸钠
(3)做氯化钠溶液的导电性实验时,小华不仅看到灯泡亮了,还观察到与电解水相似的现象:两根石墨电极上都出现了气泡.这激发了小华探究气泡成分的欲望.请你一起参与小华的探究活动吧!
[提出问题]氯化钠溶液通电时石墨电极上分别生成了什么气体?
[查阅资料]Cl2是黄绿色、有刺激性气味的有毒气体,常温下1体积水能溶解2体积Cl2.
[提出假设]假设1:电极上分别生成了氢气和氯气;
假设2:电极上分别生成了氧气和氯气;
假设3:电极上分别生成了氢气和氧气.以上假设的依据是______.
[设计实验]小华决定用右图所示的装置来电解氯化钠的饱和溶液.并收集两个电极上产生的气体.
[实验分析]观察到一支试管中收集的气体为黄绿色,另一支试管中收集到的气体能被点燃,则假设______成立:小红又向反应后的溶液中滴加无色酚酞,结果酚酞变红,请写出氯化钠溶液通电时发生反应的化学方程式_______.
[反思与评价]联想电解水的实验,你认为在电解水时______(填“可以”或“不可以”)加入少量的氯化钠溶液,原因是______.
(4)小华还想利用H2还原氧化铁的实验测定水中氢、氧两种元素的质量比.
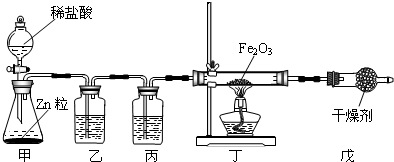
[设计实验]实验装置图如下:
①写出装置中试剂的名称:乙______,丙______.
②实验开始时,应该先______(选填字母).
a.加热反应管丁 b.从分液漏斗中滴加液体
在这两步操作之间,还应进行的一步操作是______.
③写出反应管丁中发生反应的化学方程式:______.
[进行实验]该小组同学进行了实验,测得了下列数据:
| 反应前 | 反应后 | |
| 丁管和内盛物的总质量 | 132.4g | 130.0g(冷却到室温称量) |
| 戊管及内盛物的总质量 | 143.2g | 145.9g |
[误差分析]
①如果该实验缺少装置丙,则测得的水中氢、氧两种元素的质量比会______(选填“偏大”或“偏小”).
②如果实验后观察到反应管丁中有水珠凝结,则测得的水中氢、氧两种元素的质量比会______(选填“偏大”或“偏小”). 查看习题详情和答案>>