摘要:你能将下列混合物分离吗?分别写出你的方法? ① 水和酒精的混合溶液 ② 碳粉中混有铁粉 第六章 A卷
网址:http://m.1010jiajiao.com/timu3_id_3944708[举报]
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg( b>a),则混合物中Cu2O的质量分数为
×100%
×100%.
(5)实验小组欲利用该红色粉末制取较纯净的胆矾 (CuS04.5H20).经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH 如下:
实验室有下列试剂可供选择:A.氯水 B.H2O2 C.NaOH D.Cu2(OH)2CO3
实验小组设计如下实验方案:
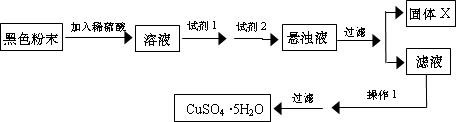
试回答:
①试剂I为
②固体X的化学式为
③操作I为
查看习题详情和答案>>
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是
溶液变为血红色
溶液变为血红色
.(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?
不合理
不合理
简述你的理由(不需写出反应的方程式 )Cu能将Fe3+还原为Fe2+
Cu能将Fe3+还原为Fe2+
.(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是
Fe2O3和Cu2O的混合物
Fe2O3和Cu2O的混合物
,写出发生反应的离子方程式Fe2O3+6H+=2Fe3++3H2O;Cu2O+2H+=Cu+Cu2++H2O;2Fe3++Cu=2Fe2++Cu2+
Fe2O3+6H+=2Fe3++3H2O;Cu2O+2H+=Cu+Cu2++H2O;2Fe3++Cu=2Fe2++Cu2+
.探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg( b>a),则混合物中Cu2O的质量分数为
| 9(b-a) |
| a |
| 9(b-a) |
| a |
(5)实验小组欲利用该红色粉末制取较纯净的胆矾 (CuS04.5H20).经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH 如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验小组设计如下实验方案:

试回答:
①试剂I为
B
B
,试剂II为D
D
(填字母).②固体X的化学式为
Fe(OH)3
Fe(OH)3
.③操作I为
加热蒸发
加热蒸发
.小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”.
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是:
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是:
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为:
(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成
②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是:
查看习题详情和答案>>
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是:
因为Fe2+中铁元素化合价处于中间价态,可以升高也可以降低
因为Fe2+中铁元素化合价处于中间价态,可以升高也可以降低
.(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是:
Cl2+2Fe2+=2Cl-+2Fe3+
Cl2+2Fe2+=2Cl-+2Fe3+
写离子方程式),可能观察到的现象是:溶液由浅绿色变为黄
黄
色.②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选
硫氰酸钾溶液
硫氰酸钾溶液
(填名称)滴入小明所得的混合液中,并通过溶液出现血红
血红
色的现象,证明小明的观点和实验方案都是正确的.③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为:
Zn Fe Cu
Zn Fe Cu
.(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成
Fe
Fe
(填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成Fe3+
Fe3+
.②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是:
加入适量铁粉
加入适量铁粉
,相关反应的离子方程式:2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”.
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是:______.
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是:______写离子方程式),可能观察到的现象是:溶液由浅绿色变为______ 色.
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选______(填名称)滴入小明所得的混合液中,并通过溶液出现______色的现象,证明小明的观点和实验方案都是正确的.
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为:______.
(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成______(填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成______.
②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是:______,相关反应的离子方程式:______.
查看习题详情和答案>>
小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”.
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是:______.
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是:______写离子方程式),可能观察到的现象是:溶液由浅绿色变为______ 色.
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选______(填名称)滴入小明所得的混合液中,并通过溶液出现______色的现象,证明小明的观点和实验方案都是正确的.
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为:______.
(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成______(填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成______.
②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是:______,相关反应的离子方程式:______.
查看习题详情和答案>>
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是:______.
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是:______写离子方程式),可能观察到的现象是:溶液由浅绿色变为______ 色.
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选______(填名称)滴入小明所得的混合液中,并通过溶液出现______色的现象,证明小明的观点和实验方案都是正确的.
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为:______.
(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成______(填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成______.
②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是:______,相关反应的离子方程式:______.
小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”.
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是: .
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是: 写离子方程式),可能观察到的现象是:溶液由浅绿色变为 色.
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选 (填名称)滴入小明所得的混合液中,并通过溶液出现 色的现象,证明小明的观点和实验方案都是正确的.
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为: .
(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成 (填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成 .
②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是: ,相关反应的离子方程式: . 查看习题详情和答案>>
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是: .
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是: 写离子方程式),可能观察到的现象是:溶液由浅绿色变为 色.
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选 (填名称)滴入小明所得的混合液中,并通过溶液出现 色的现象,证明小明的观点和实验方案都是正确的.
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为: .
(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成 (填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成 .
②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是: ,相关反应的离子方程式: . 查看习题详情和答案>>