摘要:20.为除去粗盐中的Ca2+.Mg2+.Fe3+.SO42-以及泥沙等杂质.某同学设计了一种制备精盐的实验方案.步骤如下: 称取粗盐 滤液 精盐 (1)判断BaCl2已过量的方法是 . (2)第④步中.相关的离子方程式是 . (3)若先用盐酸调pH值再过滤.将对实验结果产生影响. 其原因是 . (4)为检验精盐纯度.需配制150 mL.0.2 mol/L NaCl溶液. 右图是该同学转移溶液的示意图.图中的错误是 . 100 mL容量瓶
网址:http://m.1010jiajiao.com/timu3_id_393989[举报]
 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐
| ||
| ① |
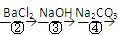
| ||
| ⑤ |
| ||
| ⑥ |
| ||
| ⑦ |
(1)判断BaCl2已过量的方法是
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
.(2)第④步中,相关的离子方程式是
Ca2++CO32-=CaCO3↓
Ca2++CO32-=CaCO3↓
;Ba2++CO32-=BaCO3↓
Ba2++CO32-=BaCO3↓
.(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
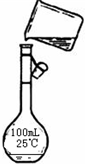
.(4)为检验精盐纯度,需配制150mL 0.2mol?L-1NaCl(精盐)溶液,右图是该同学转移溶液的示意图,图中的错误是
未用玻璃棒引流,未采用150mL容量瓶
未用玻璃棒引流,未采用150mL容量瓶
. 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下所示(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下所示(用于沉淀的试剂稍过量):称取粗盐
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
(1)判断BaCl2已过量的方法是
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
.(2)第④步中,相关的离子方程式是
Ca2++CO32-=CaCO3↓,Ba2++CO32-=BaCO3↓
Ca2++CO32-=CaCO3↓,Ba2++CO32-=BaCO3↓
.(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
.(4)为检验精盐纯度,制配制 100mL 0.2mol/L NaCl(精盐)溶液,如图所示是该同学转移溶液的示意图,图中的错误是
未用玻璃棒引流,未采用100mL容量瓶
未用玻璃棒引流,未采用100mL容量瓶
.为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐
滤液
精盐
(1)判断BaCl2已过量的方法是
(2)加入NaOH溶液的目的是
(3)第④步中,相关的化学方程式是
(4)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
查看习题详情和答案>>
称取粗盐
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸蒸发 |
| ⑥ |
| 结晶烘干 |
| ⑦ |
(1)判断BaCl2已过量的方法是
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
.(2)加入NaOH溶液的目的是
溶液中存在的 Mg2+和 Fe3+ 完全转化为沉淀除去
溶液中存在的 Mg2+和 Fe3+ 完全转化为沉淀除去
.(3)第④步中,相关的化学方程式是
Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓
Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓
.(4)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
. 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):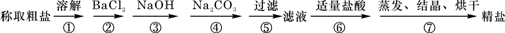
(1)第⑤步实验操作需要烧杯、
漏斗
漏斗
、玻璃棒
玻璃棒
等玻璃仪器.(2)步骤2中,判断加入BaCl2已过量的方法是:
在②步后的上层清液中,再滴入氯化钡溶液,若溶液未变浑浊,则说明所加的氯化钡已过量
在②步后的上层清液中,再滴入氯化钡溶液,若溶液未变浑浊,则说明所加的氯化钡已过量
(3)除杂试剂BaCl2、NaOH、Na2CO3、加入的顺序还可以是(用化学式回答)
NaOH、BaCl2、Na2CO3或BaCl2、NaOH、Na2CO3
NaOH、BaCl2、Na2CO3或BaCl2、NaOH、Na2CO3
.(4)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
在此酸度条件下,会有部分沉淀溶解,影响精盐的纯度
在此酸度条件下,会有部分沉淀溶解,影响精盐的纯度
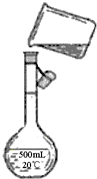
.(5)为检验精盐纯度,需配制200mL 1mol/L NaCl(精盐)溶液,如图是该同学转移溶液的示意图,图中的错误是:
未用玻璃棒引流,未使用200mL的容量瓶
未用玻璃棒引流,未使用200mL的容量瓶
(6)配制过程中,下列操作情况会使结果偏低的是
AD
AD
A.称量时,托盘天平左盘加砝码,右盘加氯化钠
B.移液前,容量瓶中有少量蒸馏水未倒出
C.定容时,俯视容量瓶刻度线观察液面
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容.
 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)称取粗盐
| ①溶解 |
| ②BaCl2 |
| ③NaOH |
| ④Na2CO3 |
| ⑤过滤 |
| ⑥适量盐酸 |
| ⑦结晶、烘干 |
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的离子方程式是
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
(4)为检验精盐纯度,特配制150mL 0.2mol?L-1 NaCl溶液,如图是该同学转移溶液的示意图,图中的错误是
(5)提纯过程中步骤①⑤⑦都用到相同的仪器,名称: