摘要:12.一种白色粉末A是由NaCl.K2SO4.Na2CO3.KHCO3和NaHCO3等五种物质中的两种组成.取少量A溶于水.进行焰色反应.火焰呈黄色.说明A中含 .若透过蓝色钴玻璃可观察到火焰呈紫色.说明A中含 ,取少量A.加入稀盐酸后.有无色略带酸味的气体生成.此气体能使澄清石灰水变浑浊.说明A中可能含有 离子或 离子,取少量A的溶液.加入BaCl2溶液.观察不到明显变化,另取少量A的溶液.加入用稀HNO3酸化的AgNO3溶液.,也没有明显的变化.说明A中一定不含 . 和 .因此.A是由 和 组成的.
网址:http://m.1010jiajiao.com/timu3_id_393651[举报]
已知A、B、C、D、E是含有一种相同元素的五种物质,他们之间可发生转化: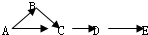 其中A是单质,B是气体,C、D是氧化物,E是最高价氧化物对应的水化物.
其中A是单质,B是气体,C、D是氧化物,E是最高价氧化物对应的水化物.
(1)如果A是一种淡黄色粉末固体,这五种物质的化学式分别是:
A
(2)如果A是一种常见的气体,这五种物质的化学式分别是:
A
查看习题详情和答案>>
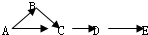 其中A是单质,B是气体,C、D是氧化物,E是最高价氧化物对应的水化物.
其中A是单质,B是气体,C、D是氧化物,E是最高价氧化物对应的水化物.(1)如果A是一种淡黄色粉末固体,这五种物质的化学式分别是:
A
S
S
,BH2S
H2S
; CSO2
SO2
; DSO3
SO3
;EH2SO4
H2SO4
.(2)如果A是一种常见的气体,这五种物质的化学式分别是:
A
N2
N2
,BNH3
NH3
; CNO
NO
; DNO2
NO2
;EHNO3
HNO3
.A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体.
(1)B、C两元素的名称为:
(2)用电子式表示C2D的形成过程:
 .
.
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,其化学方程式为
查看习题详情和答案>>
(1)B、C两元素的名称为:
氧、钠
氧、钠
;(2)用电子式表示C2D的形成过程:


(3)由B、C两元素所形成的原子个数比为1:1的化合物属于
离子
离子
(填“离子”或“共价”)化合物,存在的化学键的种类有离子键、非极性键
离子键、非极性键
,写出它与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
.(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,其化学方程式为
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.此实验中常加入一种黑色粉未物质,其作用是
| ||
催化剂
催化剂
.(14分)有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.4 mol淡黄色粉末时,产生气体0.3 mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如下图所示。
根据题意回答下列问题:
(1)淡黄色粉末为____________(填名称)。
(2)溶液中肯定有______________离子,肯定没有__________离子。
(3)溶液中各离子的物质的量之比为
________________________________________________________________________。
(4)写出下列反应方程式:
①淡黄色粉末与水反应的化学方程式:____________________________________。
②刺激性气味的气体产生的离子方程式:______________________________________。
③沉淀部分减少时的离子方程式:_______________________________________。
查看习题详情和答案>>
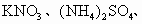
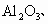
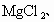
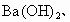 无水
无水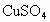 中的一种,除蒸馏水外不得使用任何其他试剂,对这些物质进行鉴别,并按要求填写下列空白.
中的一种,除蒸馏水外不得使用任何其他试剂,对这些物质进行鉴别,并按要求填写下列空白.




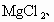
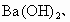 无水
无水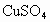 中的一种,除蒸馏水外不得使用任何其他试剂,对这些物质进行鉴别,并按要求填写下列空白.
中的一种,除蒸馏水外不得使用任何其他试剂,对这些物质进行鉴别,并按要求填写下列空白.

