摘要:2 x6.02xl023 C.标准状况下.2.24L乙烷中含有的非极性键数约为0.7x6.02xl023 D.含1mol硅原子的SiO2晶体中Si一O键的个数约为2x6.02xl023
网址:http://m.1010jiajiao.com/timu3_id_391331[举报]
由A、B两种短周期元素形成的离子化合物中,阳离子和阴离子的个数比为2:l。一个阳离子和一个阴离子的核外电子数之比为5:9,若A形成阳离子,其原子序数为x,则B的原子序数为
![]()
![]() A.x
A.x![]() 3 B.x
3 B.x![]() 6 C.x+13 D.x+10
6 C.x+13 D.x+10
①②③④⑤⑥六种元素,在元素周期表中的位置如图所示.回答下列问题:
(1)六种元素中,金属性最强的元素位置位于元素周期表
(2)元素①和②可以形成众多的化合物,其中最简单的是(写电子式)
 ,与该化合物电子总数相同的三原子分子的结构式为
,与该化合物电子总数相同的三原子分子的结构式为
(3)画出元素③的原子结构示意图
 ,该元素形成的气态氢化物通常极易溶解于水,其原因是
,该元素形成的气态氢化物通常极易溶解于水,其原因是
(4)写出元素④、⑥的最高价氧化物对应水化物相互反应的离子方程式为
查看习题详情和答案>>
| ⅠA | 0 | |||||||
| ① | ⅡA | … | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ |
第三周期ⅠA族
第三周期ⅠA族
,该元素的单质与水反应的离子方程式为2H2O+2Na═2Na++2OH-+H2↑
2H2O+2Na═2Na++2OH-+H2↑
.(2)元素①和②可以形成众多的化合物,其中最简单的是(写电子式)


H-O-H
H-O-H
.(3)画出元素③的原子结构示意图


NH3是极性分子,能与水反应,与水分子能形成氢键
NH3是极性分子,能与水反应,与水分子能形成氢键
.(4)写出元素④、⑥的最高价氧化物对应水化物相互反应的离子方程式为
H++OH-═H2O
H++OH-═H2O
.
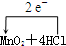 (浓)═MnCl2+Cl2↑+2H2O
(浓)═MnCl2+Cl2↑+2H2O