摘要:19.硅酸盐在自然界中分布极广.几乎在所有的硅酸盐矿物中.Si原子都和4个O原子结合成四面体的[SiO4]单元(图1.图中○表示“O .⊙表示“Si-O ).[SiO4]单元既可以是分立的.也可以和其它四面体共用顶点连接各种各样的链状结构 (1)形成硅氧四面体是硅与氧成键的一个重要特征.试再举两种含有[SiO4]单元的物质 . (2)最简单的硅酸盐是硅酸钠.硅酸钠溶液中滴入酚酞显红色.试用离子方程式解释酚酞变红的原因 .通入CO2能使上述溶液的红色褪色.离子方程式 . (3)将某些盐混进硅酸钠溶液时.此盐会向上扩散长成很漂亮的树状.且此树会保留金属离子的特征颜色.例如CuSO4·5H2O和Na2SiO3溶液发生水解反应长成蓝色的树.NiSO4·7H2O则会长成绿色的树.写出加入CuSO4·5H2O长成蓝树的离子方程式 . (4)图1为SiO44-.图2.图3所示硅酸盐离子的符号 . (5)由13个正四面体结合成的环状结构Si13O3722-离子中.其中有 个正四面体和另外的四面体共享2个顶点. 个和另外的四面体共享3个顶点.
网址:http://m.1010jiajiao.com/timu3_id_390367[举报]
 某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示.请根据其结构特点判断下列有关说法中正确的是( )
某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示.请根据其结构特点判断下列有关说法中正确的是( )①该有机物的化学式为C2H4O2
②该有机物的水溶液呈酸性且酸性比碳酸的强
③该有机物在自然界中分布很广.
查看习题详情和答案>>
人类使用最早的金属是___________(填下列选项编号,下同),其次是___________。在自然界中分布最广、含量最多的金属是___________。在空气中能形成致密氧化物保护膜的有___________,用于制取黄铜的是___________。在自然界中含量居第10位,外观像钢,被誉为“未来钢铁”的是___________。现在世界范围内应用最广泛的是___________。导电、导热性最好的金属是___________,其次是______________________。
a.Cu b.Fe c.Al d.Zn f.Ti g.Ag
查看习题详情和答案>>下列说法错误的是( )
| A、碳、硫单质在加热条件下都能与浓硝酸、浓硫酸发生反应 | B、氮氧化物、二氧化硫是形成酸雨的主要物质 | C、二氧化硫具有还原性,因此不能用浓硫酸干燥 | D、硅在自然界中主要以氧化物和硅酸盐的形式存在 |
短周期元素X、Y、Z、M、N原子序数依次增大,有关信息如下:
请回答:
(1)X2Z的电子式是
 ;M2Z中所含化学键类型是
;M2Z中所含化学键类型是
(2)Y的非金属性比N
(3)YX4的结构式为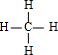
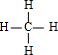 ;分子里各原子的空间分布具有
;分子里各原子的空间分布具有
(4)Y与X可形成原子个数为1:1的有机物,写出该有机物与氢气反应的方程式
查看习题详情和答案>>
| 元素 | 有关信息 |
| X | 在自然界中原子半径最小 |
| Y | 最外层电子数是次外层的2倍 |
| Z | 元素的主要化合价为-2价 |
| M | 其单质及其化合物的焰色为黄色 |
| N | 与Y同主族,其单质为半导体材料 |
(1)X2Z的电子式是


离子键
离子键
.(2)Y的非金属性比N
强
强
(填“强”或“弱”),能证明此结论的事实是CO2+H2O+SiO32-=H2SiO3↓+CO32-
CO2+H2O+SiO32-=H2SiO3↓+CO32-
(用离子方程式表示).(3)YX4的结构式为
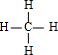
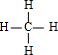
正四面体
正四面体
结构;在光照的条件下,将1mol YX4与1mol Cl2混合充分反应后,得到的产物有5
5
种.(4)Y与X可形成原子个数为1:1的有机物,写出该有机物与氢气反应的方程式
CH≡CH+H2
CH3CH3或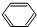 +3H2
+3H2
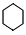
| 一定条件 |
 +3H2
+3H2| Ni |
| △ |

CH≡CH+H2
CH3CH3或 +3H2
+3H2

.| 一定条件 |
 +3H2
+3H2| Ni |
| △ |
