网址:http://m.1010jiajiao.com/timu3_id_387170[举报]
丙烯可用于合成杀除根瘤线虫的农药(分子式为C3H5Br2Cl)和应用广泛的DAP树脂: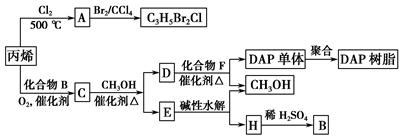
已知酯与醇可发生如下酯交换反应:
RCOOR′+R″OH催化剂△RCOOR″+R′OH(R、R′,R″代表烃基)
(1)农药C3H5Br2Cl分子中每个碳原子上均连有卤原子。
①A的结构简式是____________________________________________________,
A含有的官能团名称是________;
②由丙烯生成A的反应类型是________。
(2)A水解可得到D,该水解反应的化学方程式是_____________________________________。
(3)C蒸气密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为:碳60%,氢8%,氧32%。C的结构简式是________。
(4)下列说法正确的是(选填序号字母)________。
a.C能发生聚合反应、还原反应和氧化反应
b.C含有2个甲基的羧酸类同分异构体有4个
c.D催化加氢的产物与B具有相同的相对分子质量
d.E具有芳香气味,易溶于乙醇
(5)E的水解产物经分离最终得到甲醇和B,二者均可循环用于DAP树脂的制备。其中将甲醇与H分离的操作方法是________。
(6)F的分子式为C10H10O4。DAP单体为苯的二元取代物,且两个取代基不处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式是_______________________________________________________________。

已知酯与醇可发生如下酯交换反应:
RCOOR′+R″OH催化剂△RCOOR″+R′OH(R、R′,R″代表烃基)
(1)农药C3H5Br2Cl分子中每个碳原子上均连有卤原子。
①A的结构简式是____________________________________________________,
A含有的官能团名称是________;
②由丙烯生成A的反应类型是________。
(2)A水解可得到D,该水解反应的化学方程式是_____________________________________。
(3)C蒸气密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为:碳60%,氢8%,氧32%。C的结构简式是________。
(4)下列说法正确的是(选填序号字母)________。
a.C能发生聚合反应、还原反应和氧化反应
b.C含有2个甲基的羧酸类同分异构体有4个
c.D催化加氢的产物与B具有相同的相对分子质量
d.E具有芳香气味,易溶于乙醇
(5)E的水解产物经分离最终得到甲醇和B,二者均可循环用于DAP树脂的制备。其中将甲醇与H分离的操作方法是________。
(6)F的分子式为C10H10O4。DAP单体为苯的二元取代物,且两个取代基不处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式是_______________________________________________________________。
(1)下图是一种用于显示事物异同点的信息处理方法。例如A图中的两个圆分别代表铝和铁的有关信息,两圆重叠的区域表示铝和铁的共同点(相似点),重叠区域以外的部分表示它们独有的特征(不同点)。请你在下面横线上用化学方程式来表示与图中①②区域对应的化学性质上的不同之处(每处只要求写一个)。
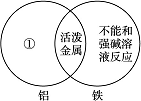 A
A
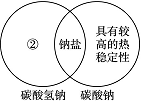 B
B
①________________________________________________________________________;
②________________________________________________________________________;
(2)为了测定铁铝合金中金属的质量分数,某校研究性学习小组设计了如下实验操作过程:称取该合金1.0g,放入烧杯中加足量盐酸,盖上表面皿,使其充分反应;反应停止,经冷却向其中加入过量NaOH溶液,充分静置后过滤,对滤出的沉淀经洗涤在空气中加热灼烧至恒重,得到固体物质1.2g。下列有关叙述不正确的是________。
A.铁的质量为0.84g
B.Al的质量分数为16%
C.加入过量NaOH溶液的目的是为了Fe2+完全沉淀
D.加入NaOH溶液后充分静置是为了保证Fe(OH)2被空气中的氧气充分氧化为Fe(OH)3
(3)Al(OH)3和NaHCO3都是治疗胃酸过多的药物,用离子方程式表示其原理,________________,______________。根据上述反应,如果是胃酸过多且有胃溃疡的患者,应该选用上述哪一种药物治疗为好________,理由是________________________。
查看习题详情和答案>>酸碱中和反应是中学化学一类重要的反应,其反应的本质都是H+和OH-反应生成H2O.某学生实验小组对课本中的两个酸碱中和实验进行了模拟研究.
(1)用下图装置进行强酸(50 mL 0.5 mol/L的HCI)和强碱(50 mL 0.55 mol/L的NaOH)反应的中和热测定.
①从实验装置上看,图中尚缺少的一种玻璃仪器是________;
②大小烧杯之间填满纸屑的作用是________;
③向组装好的量热器中加入50 mL盐酸并测定温度,取出温度计并冲
净后,再将已测定好温度的NaOH溶液50 mL加入量热器.下列加入50 mL NaOH溶液的操作正确的是________.
A.为了使酸碱充分中和,必须边滴加NaOH溶液边迅速搅拌
B.把50 mL NaOH溶液一次迅速倒入,盖上纸板迅速搅拌.
④若用醋酸代替上述盐酸实验,实验测得的中和热值________(填偏大、偏小或无影响).
(1)、用实验室准确配制的0.100 mol/L的NaOH溶液测定某未知浓度的稀盐酸.
其具体实验步骤如下:
①取一支碱式滴定管下图中有两只滴定管~上端未画出,你选择哪一只?________(填写对应字母),用少量标准NaOH溶液润洗2~3次水洗后的碱式滴定管,再加入标准的0.100 mol/L的NaOH溶液并记录液面刻度读数;
②用酸式滴定管精确的放出25.00 mL待测盐酸,置于用蒸馏水洗净的锥形瓶中,再加入酚酞(变色范围:8.2~10.0)试液2滴;
③滴定时,边滴边振荡,同进注视眼睛注视锥形瓶内容也颜色的变化,当锥形瓶内溶液由________(填写颜色变化)且半分钟内不褪色时,即达到滴定终点;
④记录液面刻度读数.根据滴定管的两次读数得出消耗标准盐酸的体积,再重复测定两次,实验结果记录见下表:

测得未知稀盐酸的物质的量浓度为________(保留小数点后3位).
⑤如果滴定结束时俯视碱式滴定管刻度读数(其它操作均正确),则对滴定结果~稀盐酸浓度的影响是________(填“偏高”、“偏低”或“无影响”).
丙烯可用于合成杀除根瘤线虫的农药(分子式为![]() )和应用广泛的DAP树脂:
)和应用广泛的DAP树脂:
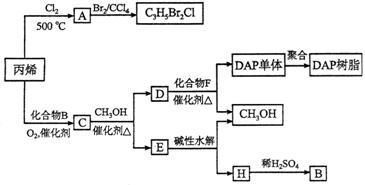
已知酯与醇可发生如下酯交换反应:
![]()
(1)农药![]() 分子中每个碳原子上均连卤原子。
分子中每个碳原子上均连卤原子。
①A结构简式是 ,A含有的官能团名称是 ;
②由丙烯生成A的反应类型是 。
(2)A水解可得到D,该水解反应的化学方程式是 。
(3)C蒸气密度是相同状态下甲烷密度的6.25倍,C中各元素的质量分数分别为:碳60%,氢8%,氧32%。C的结构简式是 。
(4)下列说法正确的是(选填序号字母) 。
a.C能发生聚合反应、还原反应和氧化反应
b.C含有2个甲基的羧酸类同分异构体有4个
c.D催化加氢的产物与B具有相同的相对分子质量
d.E具有芳香气味,易溶于乙醇
(5)E的水解产物经分离最终得到甲醇和B,二者均可循环利用于DAP树脂的制备。其中将甲醇与H分离的操作方法是 。
(6)F的分子式为![]() 。DAP单体为苯的二元取代物,且两个取代基不处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式是 。
。DAP单体为苯的二元取代物,且两个取代基不处于对位,该单体苯环上的一溴取代物只有两种。D和F反应生成DAP单体的化学方程式是 。