摘要:一定温度下在一固定容积的密闭容器中发生如下可逆反应: 2A 2C(g)在反应过程中.C的物质的量n(C)随时 间的变化关系如图所示.现从t1时刻开始对反应体系升高温度. n(C)的变化如图中qb所示. V(逆)(填“> .“= 或“< ), (2)此反应的正反应为 反应, (3)a.b两点的正反应速率:V(a) V(b)(填“> .“= 或“< ). 时间(s) 12.在100℃时.将0.200mol的N2O4气体充入2L抽空的密闭容器中.每隔一定的时间对该容器内的物质进行分析.得到如下表格: 0 20 40 60 80 100 C(N2O4) 0.100 C1 0.050 C3 a b C(NO2) 0 0.060 C2 0.120 0.120 0.120 (1)达到平衡时.N2O4的转化率为 .表中a b(填“> .“= 或“< ), (2)C1 = . 20s内N2O4的平均反应速率为 mol/ (3)若在相同情况下最初向容器中充入的是NO2气体.要达到上述同样的平衡状态.NO2的起始浓度是 .
网址:http://m.1010jiajiao.com/timu3_id_38430[举报]
一定温度下,在固定容积的密闭容器中,可逆反应:mA(气)+nB(气)?pC(气)+qD(气),当m、n、p、q为任意正整数时,下列状态:
①体系的压强不再发生变化;
②生成m molA 同时消耗q mol的D;
③各组分的物质的量浓度不再改变;
④体系的密度不再发生变化;
⑤反应速率vA:vB:vC:vD=m:n:p:q;
⑥各组分的质量分数不再改变;
⑦反应混合物中各物质的物质的量之比为m:n:p:q.
其中,一定能说明反应已达到平衡状态的是( )
①体系的压强不再发生变化;
②生成m molA 同时消耗q mol的D;
③各组分的物质的量浓度不再改变;
④体系的密度不再发生变化;
⑤反应速率vA:vB:vC:vD=m:n:p:q;
⑥各组分的质量分数不再改变;
⑦反应混合物中各物质的物质的量之比为m:n:p:q.
其中,一定能说明反应已达到平衡状态的是( )
查看习题详情和答案>>
一定温度下,在固定容积的密闭容器中,可逆反应m A(g)+nB(g)?pC(g)+qD(g),当m、n、p、q为任意正整数时,下列状态一定能说明反应已达到平衡的是( )
①体系的压强不再发生变化 ②体系的密度不再发生变化
③各组分的物质的量浓度不再改变 ④各组分的质量分数不再改变
⑤反应速率VA:VB:VC:VD=m:n:p:q.
①体系的压强不再发生变化 ②体系的密度不再发生变化
③各组分的物质的量浓度不再改变 ④各组分的质量分数不再改变
⑤反应速率VA:VB:VC:VD=m:n:p:q.
查看习题详情和答案>>
一定温度下,在固定容积的密闭容器中进行如下可逆反应:C(s) + H2O(g) 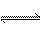 CO(g) + H2(g),当反应进行到下列情况时:①混合气体的密度不再改变 ②气体的总的物质的量不再改变 ③H2和CO的物质的量之比不再改变?④CO的质量分数不再改变 ⑤C的浓度不再改变 ⑥混合气体的平均相对分子质量不再改变。其中反应体系一定处于化学平衡状态的情况是( )
CO(g) + H2(g),当反应进行到下列情况时:①混合气体的密度不再改变 ②气体的总的物质的量不再改变 ③H2和CO的物质的量之比不再改变?④CO的质量分数不再改变 ⑤C的浓度不再改变 ⑥混合气体的平均相对分子质量不再改变。其中反应体系一定处于化学平衡状态的情况是( )
A.全部 B.除③④外 C.除③⑤⑥外 D.除⑤外
查看习题详情和答案>>
 pC(g)+qD(g),
pC(g)+qD(g),