网址:http://m.1010jiajiao.com/timu3_id_38052[举报]
下列反应中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
![]() A. NH4Cl == NH3↑+ HCl↑ B. NH3 + CO2 + H2O == NH4HCO3
A. NH4Cl == NH3↑+ HCl↑ B. NH3 + CO2 + H2O == NH4HCO3
![]() C. 2NaOH + Cl2 == NaCl + NaClO + H2O D. 2Na2O2 + 2CO2 == 2Na2CO3 + O2
C. 2NaOH + Cl2 == NaCl + NaClO + H2O D. 2Na2O2 + 2CO2 == 2Na2CO3 + O2
A、NH4Cl
| ||||
| B、2Na2O2+2CO2═2Na2CO3+O2 | ||||
| C、FeCl3+3NaOH═Fe(OH)3↓+3NaCl | ||||
D、4NH3+5O2
|
 NH3↑+HCl↑
NH3↑+HCl↑ B.NH3+CO2+H2O=NH4HCO3
C.2NaOH+Cl2=NaCl+NaClO+H2
D.2Na2O2+2CO2=2Na2CO3+O2
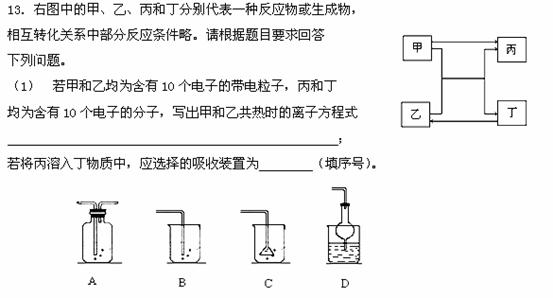
(2)若甲和乙均为含有18个电子的共价化合物,丁为黄色固体,
则甲的电子式为 ,甲中含有的化学键类型有 (填序号)。
A 离子键 B极性共价键 C 非极性共价键
(3)若甲是含有10个电子的化合物,乙是含有18个电子的单质分子,写出甲和乙反应的化学方程式 ;当乙发生反应时,转移0.1mol电子,则标况下有 L单质气体乙参加反应。
(4)若甲、乙均由两种元素组成,且含有一种相同元素,甲是含有10个电子的分子,乙是含有18个电子的分子,甲、乙发生化学反应的实验现象为 。(5)若甲和丁为非金属单质,乙和丁为非金属氧化物,则甲和丁可能为 、
(列出常见的两组的名称)。
(6)若甲、乙中均含有常见金属元素,甲为单质,乙中两元素原子的质量比为21:8,则甲、乙发生反应的化学方程式为 。
查看习题详情和答案>>