摘要:据悉我国探月工程将率先在四川西昌卫星发射中心试行.其发射火箭往往用含氮元素的肼(N2H4)作燃料.将飞船射入同步轨道.除了要精确地控制远地点发动机的点火时机之外.还要准确地校正飞船在远地点时的空间姿态.使飞船的飞行轴向入射方向完全一致.这种高科技主要靠一种新型的肼分解姿态控制发动机来解决.试回答下列有关问题: (1)氮元素位于元素周期表的第 周期.第 族. (2)液态NH3类似H2O.也能微弱电离且产生电子数相同的两种离子.则液态NH3电离方程式为 . (3)NH4NO3溶液中水的电离程度 (填“大于 .“等于 或“小于 ) NaOH溶液中水的电离程度.若将0.1mol·L-1NaOH和0.2mol·L-1 NH4NO3两溶液等体积混合所得溶液中离子浓度的大小顺序为 . (4)在结构上N2H4和NH3的关系有如H2O2和H2O的关系.N2H4能发生下列反应: N2H4+H3O+===N2H+5+H2O N2H4+H2O====N2H5++OH- N2H5++H2O====N2H62++OH- N2H5++H2O====N2H4+H3O+ 据此可得出的结论是 . A.肼水解显酸性 B.肼在水中电离出H+离子 C.肼是二元弱碱 D.肼是二元弱酸 (5)下列有关NH3.N2H4.H2O和H2O2的性质叙述正确的是 . A.H2O2对热稳定性比H2O强 B.NH3对热稳定性比水强 C.H2O2还原性比N2H4强 D.NH3结合质子的能力比水强 (6)当液态NH3与NaClO按物质的量之比为2:1进行反应时生成NaCl.肼(N2H4)和H2O.写出反应化学方程式 . (7)发射火箭时肼(N2H4)为燃料.二氧化氮作氧化剂.两者反应生成氮气和气态水.已知4g N2H4(g)在上述反应中放出71kJ的热量.写出热化学方程式 . 答案: 2NH3NH4++NH2-. (3) 大于,c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+). 2NH3+NaClO= N2H4+NaCl+H2O. (7) N2H4(g)+NO2(g)=3/2N2(g)+2H2O(g),△H=-568kJ/mol
网址:http://m.1010jiajiao.com/timu3_id_380494[举报]
2013年12月15日嫦娥三号成功登月,为我国探月工程开启新的征程.下列选项中的描述与化学研究领域无关的是( )
| A、燃料燃烧为嫦娥三号升空提供动力 | B、与地面指挥中心联系的无线电通讯 | C、月球车使用的新型镁合金等新材料 | D、高温多层隔热组件、高温合金抗氧化涂层 |
2010年lO月1日,我国成功地发射了嫦娥二号探月卫星,标志着我国探月工程进入崭新阶段.月球的矿产资源极为丰富,仅月球表面5cm厚的沙土就含有铁单质上亿吨,月球上的主要矿物有辉石(CaMgSi2O6)、斜长石(KAlSi3O8)等,下列说法或分析错误的是( )
查看习题详情和答案>>
2011年11月1日“神州八号”成功发射,它和“天宫一号”在中国甘肃、陕西上空实现对接,我国探月工程迈出重要一步。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法正确的是
A.42He原子核内含有4个质子 B.32He原子核内含有3个中子
C.32He和42He互为同位素 D. 42He具有较强的金属活动性
查看习题详情和答案>>
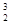 He。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列关于
He。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列关于