网址:http://m.1010jiajiao.com/timu3_id_379962[举报]
![]()
试回答:
(1)若X是强氧化性单质,则A不可能是__________(填序号,可能有一个以上正确选项)。
a.S b.N
(2)若X是常见金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为__________;C溶液在贮存时应加入少量X,理由是____________________;检验此C溶液中金属元素价态的操作方法是____________________。
(3)若A、B、C为含有金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为__________,X的化学式可能为__________(写出不同类物质)或,反应①的离子方程式为______________________________。
查看习题详情和答案>>(8分)A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。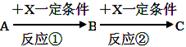
试回答:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为____ ____;C溶液在储存时应加入少量X,目的是______________________ 。
(3)若A是厨房常用的一种调味剂,则反应①的化学方程式为: ;
A与C反应可以生成一种有芳香气味的物质,该物质的结构简式为: 。
(8分)A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
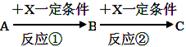
试回答:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为____ ____;C溶液在储存时应加入少量X,目的是______________________ 。
(3)若A是厨房常用的一种调味剂,则反应①的化学方程式为: ;
A与C反应可以生成一种有芳香气味的物质,该物质的结构简式为: 。
查看习题详情和答案>>

试回答:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为____ ____;C溶液在储存时应加入少量X,目的是______________________ 。
(3)若A是厨房常用的一种调味剂,则反应①的化学方程式为: ;
A与C反应可以生成一种有芳香气味的物质,该物质的结构简式为: 。

请回答下列问题:
(1)写出X与A反应的化学方程式:
| ||
| ||
(2)若试剂1是NaOH溶液,写出X与试剂1反应的离子方程式
(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是
②将物质C溶于水,其溶液呈酸性,原因是
 Al(OH)3+3H+
Al(OH)3+3H+ Al(OH)3+3H+
Al(OH)3+3H+③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以D、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是
(4)若试剂1和试剂2均是稀盐酸,将C与D混合后,通入气体Z,再滴加氢氧化钠溶液调节溶液的pH,可水解聚合得到高效净水剂聚合氯化铝铁[AlFe(OH)nCl6-n]m.气体Z是