网址:http://m.1010jiajiao.com/timu3_id_379680[举报]
(1)写出B原子的电子式
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的结构式为
(3)写出单质E与氧氧化钠溶液反应的离子方程式
(4)一定条件下,B的最高价氧化物的水化物的浓溶液与红热的木炭反应,则该反应的化学方程式
(5)在10L的密闭容器中,通入2molFC2气体和3mol C2气体,在一定条件下反应生成FC3气体.当反应达到平衡时,C2的浓度为0.21mol?L-1,则平衡时FC2的转化率为
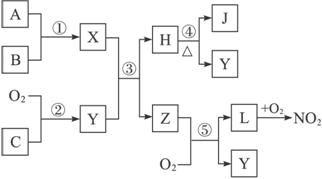
(1)用化学式表示化合物L:_____________,单质C:_____________。
(2)物质Z的分子空间结构是_____________。
(3)反应①的化学方程式为_____________________________________________。
(4)反应⑤的化学方程式为_____________________________________________。
(5)在常温下用气体密度测定NO2的相对分子质量,实验值比理论值偏(填“高”或“低”),其原因是____________________________________________________________________。
查看习题详情和答案>>(8分)A、B、C、D四种短周期元素的原子半径依次减小,在周期表中B与A、C 相邻,C的最外层电子数是其电子总数的![]() ,D能分别与A、B、C形成电子总数相等的化合物X、Y、Z。试回答:
,D能分别与A、B、C形成电子总数相等的化合物X、Y、Z。试回答:
(1)在X、Y、Z三种化合物中,沸点最高的是(用化学式表示,下同)_____________,稳定性由强到弱的顺序是___________________________________。
(2)若由A、B、C、D四种元素组成一种离子化合物,1 mol该化合物中含有10 mol原子,则该化合物受热分解的化学方程式为:___________ 。
若由A、B、C、D四种元素中的两种组成化合物,化合物中分子的空间构型为直线型。写出符合上述要求且原子数不少于3的任意两种化合物的结构式:___________________________________。
(3)Y跟HCl反应生成固体。该固体跟有毒的工业盐NaNO2的水溶液混合加热,NaNO2被完全破坏,当有1 molNaNO2发生反应时,共有3 mol电子转移,该反应的化学方程式为_________________________。
查看习题详情和答案>>
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)写出F在周期表中的位置________。画出D的离子结构示意图___________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_______________。1gA的单质与C的单质完全反应生成Y(Y为液态),放出142.9KJ的热量,请写出该反应的热化学方程式_______________________。
(3)C与F形成的常见化合物属于_________晶体。若E的单质是常见的半导体材料,则A与B形成的常见化合物R、C与D形成的常见化合物S、C与E 形成的常见化合物T, R、S、T三者的沸点从高到低排列为___________________________(写化学式)。
(4)画出B单质的结构式_______________。最近科学家合成出了B元素形成的B![]() 电子式
电子式, 则n值为___ 。
(5)A的单质与C的单质在KOH的溶液中可以形成原电池,已知M、N均为碳电极,在电池的M极通入A的单质气体,N极通入C的单质气体,则N极的电极反应式为____________________________________。
(6)在10L的密闭容器中,通入2molFC2气体和3mol C的气体单质,一定条件下反应后生成FC3气体,当反应达到平衡时,单质C的浓度为0.21mol·L—1,则平衡时FC2的转化率为________。
查看习题详情和答案>>
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)写出F在周期表中的位置________。画出D的离子结构示意图___________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_______________。1gA的单质与C的单质完全反应生成Y(Y为液态),放出142.9KJ的热量,请写出该反应的热化学方程式_______________________。
(3)C与F形成的常见化合物属于_________晶体。若E的单质是常见的半导体材料,则A与B形成的常见化合物R、C与D形成的常见化合物S、C与E 形成的常见化合物T, R、S、T三者的沸点从高到低排列为___________________________(写化学式)。
(4)画出B单质的结构式_______________。最近科学家合成出了B元素形成的B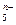 电子式
电子式 ,则n值为___ 。
,则n值为___ 。
(5)A的单质与C的单质在KOH的溶液中可以形成原电池,已知M、N均为碳电极,在电池的M极通入A的单质气体,N极通入C的单质气体,则N极的电极反应式为____________________________________。
(6)在10L的密闭容器中,通入2molFC2气体和3mol C的气体单质,一定条件下反应后生成FC3气体,当反应达到平衡时,单质C的浓度为0.21 mol·L—1,则平衡时FC2的转化率为________。