摘要:在密闭容器中.反应SO2(g)+NO2(g)NO(g)+ SO3(g) 达到平衡后.往容器中通入少量的O2.此时将会发生的变化是( ) A.容器内压强增大.平衡向逆反应方向移动 B.容器内压强不变.平衡向正反应方向移动 C.容器内压强增大.平衡不移动 D.容器内压强不变.平衡向逆反应方向移动
网址:http://m.1010jiajiao.com/timu3_id_379146[举报]
反应SO2(g)+ NO2(g)SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,试求:在该温度下。
(1)此反应的平衡常数。
(2)若SO2(g)的初始浓度增大到3mol/L, NO2(g)的初始浓度仍为2mol/L,则SO2(g)、NO2(g)的转化率变为多少?
查看习题详情和答案>>
反应SO2(g)+ NO2(g) 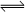 SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,试求:在该温度下。
SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,试求:在该温度下。
(1)此反应的平 衡常数。
衡常数。
(2)若SO2(g)的初始浓度增大到3mol/L, NO2(g)的初始浓度仍为2mol/L,则SO2(g)、NO2(g)的转化率变为多少?
反应SO2(g)+ NO2(g)
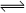 SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,试求:在该温度下。
SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,试求:在该温度下。
(1)此反应的平衡常数。
(2)若SO2(g)的初始浓度增大到3mol/L, NO2(g)的初始浓度仍为2mol/L,则SO2(g)、NO2(g)的转化率变为多少?
查看习题详情和答案>>
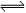 SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,试求:在该温度下。
SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,试求:在该温度下。 衡常数。
衡常数。