摘要:29. I.600℃.在密闭容器中加入一定量的Na2SO4固体使其发生以下反应并达到平衡 Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g),ΔH<0. 在恒温恒容时回答以下问题: (1)向容器分别加入以下物质.对平衡有无影响.有影响的应写出平衡移动的方向. ①加入Na2SO4 ,②加入焦炭 .③增大压强 . (2)若将容器温度再升高100℃.H2在混合气体中的含量会 . (3)若刚开始加入的Na2SO4是1.42g.平衡时容器中固体物质的质量是1.10g.Na2SO4的转化率是 . II.105Pa.500℃时.相同物质的量的SO2.O2.SO3组成的混合气体.在温度和压强不变的情况下反应且达到平衡状态.若平衡后混合气体的密度比反应前减少了.平衡时的混合气体的平均相对分子质量是 .
网址:http://m.1010jiajiao.com/timu3_id_376392[举报]
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.| 化合物 | 相对分子质量 | 密度/g?cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
I乙酸正丁酯粗产品的制备
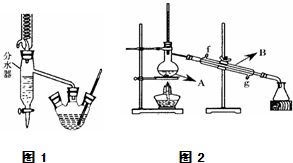
在三孔圆底烧瓶中装入沸石,加入18.5mL正丁醇和15.4mL冰醋酸(稍过量),再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)本实验过程中可能产生多种有机副产物,请写出其中一种的结构简式
CH3CH2CH2CH2OCH2CH2CH2CH3或CH2=CHCH2CH3
CH3CH2CH2CH2OCH2CH2CH2CH3或CH2=CHCH2CH3
.(2)反应时加热有利于提高酯的产率,但实验发现温度过高酯的产率反而降低,可能的原因是
乙酸、正丁醇都易挥发,温度过高可能使乙酸、正丁醇大量挥发使产率降低,温度过高可能发生副反应使产率降低;
乙酸、正丁醇都易挥发,温度过高可能使乙酸、正丁醇大量挥发使产率降低,温度过高可能发生副反应使产率降低;
.Ⅱ乙酸正丁酯粗产品的制备
(1)将圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,该步操作的目的是
溶解正丁醇;中和乙酸;降低乙酸正丁酯的溶解度,便于分层析出;
溶解正丁醇;中和乙酸;降低乙酸正丁酯的溶解度,便于分层析出;
.(2)将酯层采用如图1所示装置蒸馏.
①图2中仪器A、B的名称分别为
蒸馏烧瓶、冷凝管
蒸馏烧瓶、冷凝管
.②蒸馏收集乙酸正丁酯产品时,应将温度控制在
126.1℃
126.1℃
左右.Ⅲ计算产率
称量制得的乙酸正丁酯的质量为13.92g,则乙酸正丁酯的产率为
60%
60%
.有机合成在制药工业上有着极其重要的地位。现用硝基苯制取苯胺,再用苯胺
制得无色晶体乙酰苯胺(具有退热镇痛作用的药物)。
① 化学原理![]() 为:
为:
苯胺 乙酸 乙酰苯胺
② 相关物质的物理常数
| 物 质 | 相对分 子质量 | 状 态 | 熔点 (℃) | 沸点 (℃) | 溶 解 度(g) | |
| 水 | 乙 醇 | |||||
| 苯 胺 | 93 | 无色液体 | -6 | 184 | 3.42(20℃) | 任意比混溶 |
| 冰醋酸 | 60 | 无色液体 | 17 | 118 | 任意比混溶 | 任意比混溶 |
| 乙酰苯胺 | 135 | 白色片 状固体 | 114 | 304 | 0.56(20℃)、3.45(50℃) 5.20(100℃) | 36.9(20℃) |
③ 制备乙酰苯胺的装置如右下图所示:
④ 制备方法和过程:


 已知:I苯胺易被氧化,加入少量锌可防止氧化
已知:I苯胺易被氧化,加入少量锌可防止氧化
II韦氏分馏柱作用与原理类似于冷凝管
请回答以下问题:
(1)步骤1中保持柱顶温度约为105℃,则锥形瓶中收集到的馏
分主要是 。
(2)步骤2中将反应液倒入水中的目的是 。
(3)步骤3中洗涤剂最好选择 。
A.冷水 B.热水 C.15%的乙醇溶液 D.NaOH溶液
(4)步骤4重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→ →冷却结晶→抽滤→洗涤→干燥。
(5)上述制备过程的产率是 。
查看习题详情和答案>>实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
请回答有关问题.
I乙酸正丁酯粗产品的制备
在三孔圆底烧瓶中装入沸石,加入18.5mL正丁醇和15.4mL冰醋酸(稍过量),再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)本实验过程中可能产生多种有机副产物,请写出其中一种的结构简式______.
(2)反应时加热有利于提高酯的产率,但实验发现温度过高酯的产率反而降低,可能的原因是______.
Ⅱ乙酸正丁酯粗产品的制备
(1)将圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,该步操作的目的是______.
(2)将酯层采用如图1所示装置蒸馏.
①图2中仪器A、B的名称分别为______.
②蒸馏收集乙酸正丁酯产品时,应将温度控制在______左右.
Ⅲ计算产率
称量制得的乙酸正丁酯的质量为13.92g,则乙酸正丁酯的产率为______.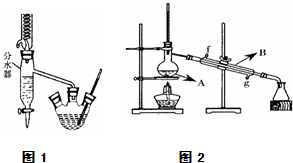
查看习题详情和答案>>
| 化合物 | 相对分子质量 | 密度/g-cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
I乙酸正丁酯粗产品的制备
在三孔圆底烧瓶中装入沸石,加入18.5mL正丁醇和15.4mL冰醋酸(稍过量),再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)本实验过程中可能产生多种有机副产物,请写出其中一种的结构简式______.
(2)反应时加热有利于提高酯的产率,但实验发现温度过高酯的产率反而降低,可能的原因是______.
Ⅱ乙酸正丁酯粗产品的制备
(1)将圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,该步操作的目的是______.
(2)将酯层采用如图1所示装置蒸馏.
①图2中仪器A、B的名称分别为______.
②蒸馏收集乙酸正丁酯产品时,应将温度控制在______左右.
Ⅲ计算产率
称量制得的乙酸正丁酯的质量为13.92g,则乙酸正丁酯的产率为______.
