摘要:4.下列说法中.错误的是 A. 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 B. 0.5 mol Ba(OH)2与0.5 mol H2SO4完全反应生成BaSO4沉淀时放出的热叫做中和热 C. △H>0表示吸热反应.△H<0表示放热反应 D. 热化学方程式中的化学计量数表示物质的量.可以是分数
网址:http://m.1010jiajiao.com/timu3_id_375040[举报]
下列说法中,错误的是
A.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
B.在稀溶液中0.5 mol Ba(OH)2与0.5 mol H2SO4完全反应生成BaSO4沉淀时放出的热可叫做中和热
C.ΔH>0表示吸热反应,ΔH<0表示放热反应
D.热化学方程式中的化学计量数表示物质的量,可以是分数
查看习题详情和答案>>用酸性氢氧燃料电池电解饱和食盐水的装置如图所示(a、b为石墨电极,不考虑U形管
中气体的溶解且a上产生的气体全部进入小试管中)。下列说法中错误的是( )
| A.同温同压下,燃料电池中参与反应的H2和O2的体积之比为2∶1 |
| B.同等条件下,U形管a、b两端产生的气体的密度之比为35.5∶1 |
| C.燃料电池中消耗0.2 g H2时,U形管中阴极产生的气体为2.24 L(标准状况下) |
| D.燃料电池中消耗1 mol O2时,小试管中反应转移的电子数约为4×6.02×1023 |
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示(a、b为石墨电极,不考虑U形管
中气体的溶解且a上产生的气体全部进入小试管中)。下列说法中错误的是( )
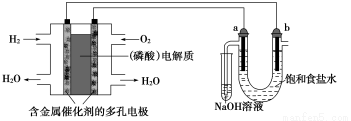
A.同温同压下,燃料电池中参与反应的H2和O2的体积之比为2∶1
B.同等条件下,U形管a、b两端产生的气体的密度之比为35.5∶1
C.燃料电池中消耗0.2 g H2时,U形管中阴极产生的气体为2.24 L(标准状况下)
D.燃料电池中消耗1 mol O2时,小试管中反应转移的电子数约为4×6.02×1023
查看习题详情和答案>>
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示(a、b为石墨电极,不考虑U形管
中气体的溶解且a上产生的气体全部进入小试管中)。下列说法中错误的是( )
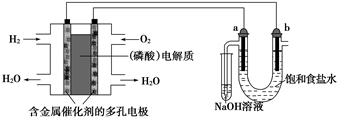
中气体的溶解且a上产生的气体全部进入小试管中)。下列说法中错误的是( )

| A.同温同压下,燃料电池中参与反应的H2和O2的体积之比为2∶1 |
| B.同等条件下,U形管a、b两端产生的气体的密度之比为35.5∶1 |
| C.燃料电池中消耗0.2 g H2时,U形管中阴极产生的气体为2.24 L(标准状况下) |
| D.燃料电池中消耗1 mol O2时,小试管中反应转移的电子数约为4×6.02×1023 |
 (2010?江苏二模)以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线,主要工艺有以下几种:
(2010?江苏二模)以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线,主要工艺有以下几种:(1)甲烷的部分氧化.其反应式如下:
CH4(g)+
| 1 |
| 2 |
则该反应的△S
>
>
0(填“>”、“<”或“=”).有研究认为甲烷部分氧化的机理为:
①CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H1=-890.3kJ?mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g);△H2=247.3kJ?mol-1
③CH4(g)+H2O(g)=CO(g)+3H2(g);△H3=
250.3
250.3
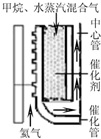
kJ?mol-1(2)甲烷水蒸汽催化重整.如右上图所示热氦气从下部流入提供能量.由甲烷和水蒸汽混合气从催化管的上部流入,从下端出来后再向上进入中心管.根据下表数据计算甲烷的转化率为
55%
55%
.| 气体 | 进口温度/℃ | 进口压强/MPa | 进口流量/g?s-1 | 出口流量/g?s-1 |
| 甲烷 | 464 | 4.26 | 12 | 5.4 |
温度过高催化剂失去活性或甲烷在高温条件下分解产生炭黑影响该反应速率
温度过高催化剂失去活性或甲烷在高温条件下分解产生炭黑影响该反应速率
.(4)甲烷的部分氧化与重整耦合.以天然气为燃料的发电尾气(主要含CO2、H2O、O2 和N2)与甲烷可直接用于制合成气.下列说法错误的是
C
C
(填序号).A.直接利用烟气中的CO2,可以大规模地减少 CO2的排放量
B.发电尾气的出口温度较高,可以利用以节约能量
C.使用恰当的催化剂可以增大甲烷的转化率
D.因发电尾气反应中包含甲烷燃烧,可实现部分热量自供,可降低成本.