摘要:14.下列结论可靠的是 A.试液eq \o(\s\up 2(滴入BaCl2溶液-- -----→白色沉淀eq \o(\s\up 2(加稀盐酸-- -----→沉淀不溶解 结论:试液中一定含SO42- B.气体eq \o(\s\up 2(点燃----→无色气体eq \o(\s\up 2(通入Ba(OH-- --------→白色沉淀 结论:原气体一定是CO C.溶液eq \o(\s\up 2(开启瓶塞-- -----→冒白雾eq \o(\s\up 2(用蘸有浓氨水的玻璃棒靠近-- -------------→白烟 结论:原溶液一定是浓盐酸 D.有色溶液eq \o(\s\up 2(滴加KSCN溶液-- -------→红色溶液 结论:原溶液中一定含Fe3+
网址:http://m.1010jiajiao.com/timu3_id_374931[举报]
下列结论可靠的是( )
查看习题详情和答案>>
A.试液
结论:试液中一定含SO42- | ||||
B.气体
结论:原气体一定是CO | ||||
C.溶液
结论:原溶液一定是浓盐酸 | ||||
D.有色溶液
结论:原溶液中一定含Fe3+ |
下列结论可靠的是
- A.试液
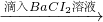 白色沉淀
白色沉淀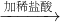 沉淀不溶解
沉淀不溶解
结论:试液中一定含SO42- - B.气体
 无色气体
无色气体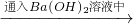 白色沉淀
白色沉淀
结论:原气体一定是CO - C.溶液
 冒白雾
冒白雾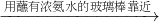 白烟
白烟
结论:原溶液一定是浓盐酸 - D.有色溶液
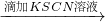 变红色
变红色
结论:原溶液中一定含Fe3+
(2013?上海二模)下列根据实验操作和现象所得出的结论可靠的是( )
|
查看习题详情和答案>>
为了确定SbCl3、SbCl5、SnCl4是否为离子化合物,可以进行下列实验,其中合理、可靠的是( )
A.观察常温下的状态,SbCl5是苍黄色液体,SnCl4为无色液体。结论:SbCl5和SnCl4都是离子化合物
B.测定SbCl3、SbCl5、SnCl4的熔点依次为73.5℃、2.8℃、-33℃。结论:SbCl3、SbCl5、SnCl4都不是离子化合物
C.将SbCl3、SbCl5、SnCl4溶解于水中,滴入HNO3酸化的AgNO3溶液,产生白色沉淀。结论:SbCl3、SbCl5、SnCl4都是离子化合物
D.测定SbCl3、SbCl5、SnCl4的水溶液的导电性,发现它们都可以导电。结论:SbCl3、SbCl5、SnCl4都是离子化合物
查看习题详情和答案>>