摘要:15mL NO2和NH3的混合气体在一定条件下发生反应:6NO2 + 8NH3 = 7N2 + 12H2O 已知参加反应的NH3比NO2多1mL.则原混合气体中NO2与NH3的体积比为 A.3:4 B.3:5 C.5:7 D.1:4或11:4
网址:http://m.1010jiajiao.com/timu3_id_374382[举报]
为消除NO和NO2对大气的污染,常用碱溶液吸收其混合气。有m mol NO2和n mol NO组成的混合气体,用NaOH溶液将其完全吸收,无气体剩余。现有浓度为a mol·L-1的NaOH溶液,则需此NaOH 溶液的体积是( )
A.![]() L B.
L B.![]() L C.
L C.![]() L D.
L D.![]() L
L
已知氮的氧化物跟NaOH溶液发生的化学反应如下:
3NO2+2NaOH=2NaNO3+NO↑+H2O; NO2+NO+2NaOH=2NaNO2+H2O;现有m mol NO2和n mol NO组成的混合气体,要用NaOH溶液使其完全吸收无气体剩余,现有浓度为a mol/L的NaOH溶液,则需此NaOH溶液的体积为( )
A. L L | B. L L | C. L L | D.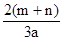 L L |
已知氮的氧化物跟NaOH溶液发生的化学反应如下:
3NO2+2NaOH=2NaNO3+NO↑+H2O; NO2+NO+2NaOH=2NaNO2+H2O;现有m mol NO2和n mol NO组成的混合气体,要用NaOH溶液使其完全吸收无气体剩余,现有浓度为a mol/L的NaOH溶液,则需此NaOH溶液的体积为( )
A. L B.
L B. L C.
L C. L D.
L D. L
L
查看习题详情和答案>>
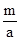 L B.
L B. 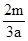 L
C.
L
C. 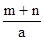 L
D.
L
D. 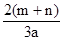 L
L