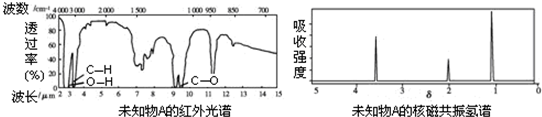
摘要:17.有三根平行的弹性绳A.B.C.其左端分布在同一直线M.N上.让它们的左端同时开始振动.经过一定时间后出现了右图所示情况.其中P.Q是平行于M.N的一条参考线.由图中信息可知 A.形成的三列波的传播速度相同 B.形成的三列波的波长相同 C.弹性绳A中的质点振动的频率最大 D.弹性绳A中的质点振动的周期最大
网址:http://m.1010jiajiao.com/timu3_id_372904[举报]
Ⅰ右图中A、B、C、D四条曲线是表示ⅣA、ⅤA、ⅥA、ⅦA族元素的气态氢化物的沸点变化曲线,其中A、D分别表示________、________族元素气态氢

化物的沸点变化;同一族中第3、4、5周期元素的气态氢化物沸点依次升高,其原因是________;
图中第2周期有三种元素的气态氢化物沸点显著高于相应的同族第3周期元素气态氢化物的沸点,其原因是________
Ⅱ.已知氨分子内键与键的夹角约为107o18’.从反应NH3+H+→NH4+可知:NH4+中有一根键比较特殊,其结构可表示为A式.但是,虽然有一根键形成过程与众不同,而其结果是完全相同的,都是N、H原子间共用一对电子,键与键的夹角均为109o28’.故NH4+的结构也可表示为B式.

(1)还有一些你熟悉的分子或离子中,也存在上述特殊共价键,如:________等.
(在下列微粒中选择填空:[Ag(NH3)2]+,PCl5,Fe(SCN)3,NH3·H2O,H3O+)
(2)写出H3O+的电子式________;你认为H3O+中键与键的夹角与下列哪个角度最接近?________
A、120o
B、109o28'
C、107o18'
D、60o
(3)氮化硼(BN)是一种新型无机非金属材料,它有两种晶型:金刚石晶型和石墨晶型.其中,金刚石晶型的氮化硼材料具有硬度大、熔点高等特性,它的结构中也含有上述特殊共价键.则:在金刚石晶型的氮化硼中,每个硼原子与________个氮原子以B─N键连接,原子间相互连接的最小的环上有________个氮原子和________个硼原子.
在一次学生实验中,学生用铝片分别和稀盐酸、稀硫酸反应,发现:铝片与稀盐酸反应现象非常明显,而和稀硫酸几乎不反应.这和教材中“铝能跟稀盐酸或稀硫酸反应生成氢气“的说法不一致.为排除因试剂变质等因素造成的影响,该学生在教师的指导下重新进行下列实验,验证是否存在上述现象.
实验用品:仪器(略,凡是实验需要的都有)
药品:3.0mol?L-1盐酸、1.5mol?L-1硫酸、3.0mol?L-1硫酸,相同大小的铝片(纯度>99.5%)
实验过程:往三根相同的试管中分别加入相同的铝片各一片,再往试管中分别加入等体积的3.0mol?L-1盐酸、1.5mol?L-1硫酸、3.0mol?L-1硫酸,观察反应进行到1,2,5,15,20分钟时的铝与酸反应的情况.结果如下:
通过上述实验可知,无论是用1.5mol?L-1硫酸还是3.0mol?L-1硫酸,均无明显的现象,而3.0mol?L-1盐酸与铝片反应的现象却十分明显.
(1)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是
(2)根据以上探究“铝与稀盐酸和稀硫酸反应差异的原因”,你能对问题原因作出哪些假设或猜想(列出两种即可)?
假设一:
假设二:
查看习题详情和答案>>
实验用品:仪器(略,凡是实验需要的都有)
药品:3.0mol?L-1盐酸、1.5mol?L-1硫酸、3.0mol?L-1硫酸,相同大小的铝片(纯度>99.5%)
实验过程:往三根相同的试管中分别加入相同的铝片各一片,再往试管中分别加入等体积的3.0mol?L-1盐酸、1.5mol?L-1硫酸、3.0mol?L-1硫酸,观察反应进行到1,2,5,15,20分钟时的铝与酸反应的情况.结果如下:
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 3.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
| 3.0mol/L硫酸 | 均无明显现象(无气泡产生) | ||||
(1)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是
反应放出热量,温度升高,使化学反应速率加快
反应放出热量,温度升高,使化学反应速率加快
.(2)根据以上探究“铝与稀盐酸和稀硫酸反应差异的原因”,你能对问题原因作出哪些假设或猜想(列出两种即可)?
假设一:
促进金属铝表面的氧化膜与H+反应
促进金属铝表面的氧化膜与H+反应
假设二:
对金属铝表面的氧化膜与H+反应对起阻碍作用
对金属铝表面的氧化膜与H+反应对起阻碍作用
.已知某有机物A的红外光谱和核磁共振氢谱如图,下列说法不正确的是( )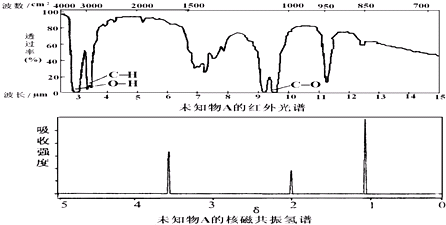

| A、由红光外谱可知,该有机物中至少有三种不同的化学键 | B、仅由其核磁共振氢谱无法得知其分子中的氢原子总数 | C、若A的化学式为C3H6O,则其结构简式为CH3COCH3 | D、由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子 |
(2010?抚顺一模)芳香酯类化合物A、B互为同分异构体,均含C、H、O三种元素.相同状况下,A、B蒸气对氢气的相对密度是97,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍.
(1)A的分子式是
(2)完全燃烧时,1mol D与1mol 下列
a.C3H6O3 b.C3H8O c.C2H4 d.C2H6O2
(3)B的结构简式是
 .水杨酸与小苏打反应的化学方程式是
.水杨酸与小苏打反应的化学方程式是
 .C与F反应的化学方程式是
.C与F反应的化学方程式是
(4)同时符合下列要求的同分异构体有三种.即:①与A互为同分异构体②可以水解③苯环上有两个取代基,且苯环上的一氯代物只有1种.已知其中一种的结构简式为: ,请写出另外两种同分异构体的结构简式
,请写出另外两种同分异构体的结构简式 、
、
 、
、 .
.
查看习题详情和答案>>

(1)A的分子式是
C10H10O4
C10H10O4
.已知:各有机物间存在如下转化关系其中C能发生银镜反应,F经连续氧化可生成C;C与D是相对分子质量相同的不同类有机物.(2)完全燃烧时,1mol D与1mol 下列
a、c
a、c
的耗氧量相同(填字母代号).a.C3H6O3 b.C3H8O c.C2H4 d.C2H6O2
(3)B的结构简式是




CH3OH+HCOOH
HCOOCH3+H2O
| 浓硫酸 |
| △ |
CH3OH+HCOOH
HCOOCH3+H2O
,| 浓硫酸 |
| △ |
(4)同时符合下列要求的同分异构体有三种.即:①与A互为同分异构体②可以水解③苯环上有两个取代基,且苯环上的一氯代物只有1种.已知其中一种的结构简式为:
 ,请写出另外两种同分异构体的结构简式
,请写出另外两种同分异构体的结构简式 、
、
 、
、