网址:http://m.1010jiajiao.com/timu3_id_371777[举报]
(13分)有机物A(C10H20O2)具有兰花香味。已知:
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 ▲ (选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是 ▲ 、 ▲ 。
(3)写出与D、E具有相同官能团所有同分异构体的结构简式:
▲ 。
(4)B与E反应生成A的化学反应方程式 ▲
(5)某学生检验C的官能团时,取1mol/LCuSO4溶液和2mol/LNaOH溶液各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL40%的C,加热后无红色沉淀出现。该同学实验失败的原因可能是 ▲ (选填序号)
①加入的C过多 ②加入的C太少
③加入CuSO4溶液的量过多 ④加入CuSO4溶液的量不够
查看习题详情和答案>>
(13分)有机物A(C10H20O2)具有兰花香味。已知:
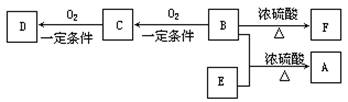
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 ▲ (选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是 ▲ 、 ▲ 。
(3)写出与D、E具有相同官能团所有同分异构体的结构简式:
▲ 。
(4)B与E反应生成A的化学反应方程式 ▲
(5)某学生检验C的官能团时,取1mol/LCuSO4溶液和2mol/LNaOH溶液各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL40%的C,加热后无红色沉淀出现。该同学实验失败的原因可能是 ▲ (选填序号)
①加入的C过多 ②加入的C太少
③加入CuSO4溶液的量过多 ④加入CuSO4溶液的量不够
查看习题详情和答案>>
(13分)有机物A(C10H20O2)具有兰花香味。已知: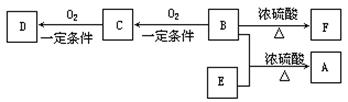
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 ▲ (选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是 ▲ 、 ▲ 。
(3)写出与D、E具有相同官能团所有同分异构体的结构简式:
▲ 。
(4)B与E反应生成A的化学反应方程式 ▲
(5)某学生检验C的官能团时,取1mol/LCuSO4溶液和2mol/LNaOH溶液各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL40%的C,加热后无红色沉淀出现。该同学实验失败的原因可能是 ▲ (选填序号)
①加入的C过多 ②加入的C太少
③加入CuSO4溶液的量过多 ④加入CuSO4溶液的量不够
( 13分)
醋柳酯是一种镇咳祛痰药。用于上呼吸道感染、感冒咳嗽、急慢性支气管炎症等的治疗,其结构简式如右。回答下列问题:
(1)醋柳酯的分子式为 。
(2)关于醋柳酯说法正确的是为( )
A.是高分子化合物 B.可与氢气发生加成反应
C.不能发生银镜反应 D.能发生水解反应且只生成2种有机物
(3)醋柳酯可由下图所示路线合成
①中间产品C中混有反应物A和B,检验C中含有A的反应可以是(用化学反应方程式表示)
②写出C和足量NaOH溶液反应的化学方程
③A的同分异构体很多,写出属于酯类,且能与FeCl3反应显紫色的同分异构体的结构简式 。
查看习题详情和答案>>
(共13分)叠氮化合物应用广泛,如NaN3,可用于汽车安全气囊,PhCH2N3可用于合成化合物V(见下图,仅列出部分反应条件,Ph-代表苯基 )
(1)下列说法不正确的是 (填字母)。
A.反应①、④属于取代反应
B.化合物I可生成酯,但不能发生氧化反应
C.一定条件下化合物Ⅱ能生成化合物I
D.一定条件下化合物Ⅱ能与氢气反应,反应类型与反应②相同
(2)化合物Ⅱ发生聚合反应的化学方程式为 (不要求写出反应条件)
(3)反应③的化学方程式为 (要求写出反应条件)
(4)化合物Ⅲ与PhCH2N3发生环加成反应生成化合物V,不同条件下环加成反应还可生成化合物V的同分异构体。该同分异构体的分子式为
, 结构简式为 。
(5)科学家曾预言可合成C(N3)4。其可分解成单质,用作炸药。有人通过NaN3与NC-CCl3反应成功合成了该物质。下列说法正确的是 (填字母)
A.该合成反应可能是取代反应
B.C(N3)4与甲烷具有类似的空间结构
C.C(N3)4不可能与化合物III发生环加成反应
D.C(N3)4分解爆炸的化学反应方程式可能为:C(N3)4→C+6N2↑
查看习题详情和答案>>