摘要: 溴乙烷在不同溶剂中与NaOH发生不同类型的反应.生成不同的反应产物.某同学依据溴乙烷的性质.用右图实验装置验证 取代反应和消去反应的产物.请你一起参与探究. 实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷.振荡. 实验操作II:将试管如图固定后.水浴加热. (1)用水浴加热而不直接用酒精灯加热的原因是 . (2)观察到 现象时.表明溴乙烷与NaOH溶液已完全反应. (3)鉴定生成物中乙醇的结构.可用的波谱是 . (4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应.在你设计的实验方案中.需要检验的是 .检验的方法是 (需说明:所用的试剂.简单的实验操作及预测产生的实验现象).
网址:http://m.1010jiajiao.com/timu3_id_371677[举报]
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL溴乙烷,振荡.
实验操作Ⅱ:将试管如图固定后,水浴加热.
(1)用水浴加热而不直接用酒精灯加热的原因是
使试管受热均匀
使试管受热均匀
;试管口安装一长导管的作用是溴乙烷沸点低,减少溴乙烷的损失
溴乙烷沸点低,减少溴乙烷的损失
.(2)观察到
试管内溶液静置后不分层
试管内溶液静置后不分层
现象时,表明溴乙烷与NaOH溶液已完全反应.(3)鉴定生成物中乙醇的结构,可用的波谱是
红外光谱
红外光谱
,核磁共振氢谱
核磁共振氢谱
.(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是
生成的气体
生成的气体
,检验的方法是将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,酸性KMnO4溶液褪色(或直接通入溴的四氯化碳溶液)
将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,酸性KMnO4溶液褪色(或直接通入溴的四氯化碳溶液)
(需说明所用的试剂、简单的实验操作及预测产生的实验现象).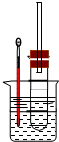 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL 溴乙烷,振荡.
实验操作II:将试管如图固定后,水浴加热.
(1)用水浴加热而不直接用酒精灯加热的原因是
溴乙烷沸点低,减少溴乙烷的损失
溴乙烷沸点低,减少溴乙烷的损失
.(2)观察到
试管内溶液静置后不分层
试管内溶液静置后不分层
现象时,表明溴乙烷与NaOH溶液已完全反应.(3)鉴定生成物中乙醇的结构,可用的波谱是
核磁共振氢谱
核磁共振氢谱
.(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是
乙烯
乙烯
,检验的方法是将生成的气体先通过盛有水的试管,再通入盛有KMnO4溶液的试管,KMnO4溶液褪色(或直接通入溴的四氯化碳溶液,溴水褪色)
将生成的气体先通过盛有水的试管,再通入盛有KMnO4溶液的试管,KMnO4溶液褪色(或直接通入溴的四氯化碳溶液,溴水褪色)
(需说明:所用的试剂、简单的实验操作及预测产生的实验现象).溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.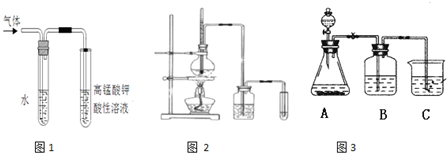
反应类型
(2)写出溴乙烷在NaOH乙醇溶液中的反应方程式
图2是实验室制乙烯并检验其性质的装置图,请回答:
(1)写出圆底烧瓶中反应的方程式
(2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式:
(3)为了检验乙烯的生成,试管中应盛放
(4)洗瓶中盛放的试剂为
某学习小组同学为了确定盐酸、苯酚、碳酸的酸性强弱,设计了如图3所示的装置图进行实验:
(1)锥形瓶内装某可溶性盐,写出A中反应的离子方程式:
(2)C中的现象为
(3)B中的试剂为
查看习题详情和答案>>

反应类型
取代
取代
.某同学取少量溴乙烷与NaOH水溶液反应后的混合溶液,向其中滴加AgNO3 溶液,加热,产生少量沉淀.该同学由此得出溴乙烷与NaOH水溶液反应,生成了溴化钠,你认为是否合理,原因:不合理没有用硝酸中和氢氧化钠溶液
不合理没有用硝酸中和氢氧化钠溶液
.(2)写出溴乙烷在NaOH乙醇溶液中的反应方程式
CH2BrCH3+NaOH
CH2=CH2↑+H2O+NaBr
| 醇 |
| 加热 |
CH2BrCH3+NaOH
CH2=CH2↑+H2O+NaBr
反应类型| 醇 |
| 加热 |
消去反应
消去反应
.反应中生成的气体可以用图1所示装置检验,现象是溶液褪色
溶液褪色
,水的作用是吸收乙醇
吸收乙醇
.除高锰酸钾酸性溶液外,还可以用溴的四氯化碳溶液
溴的四氯化碳溶液
检验生成的气体,此时还有必要将气体先通入水中吗?没有
没有
(填“有”或“没有”)图2是实验室制乙烯并检验其性质的装置图,请回答:
(1)写出圆底烧瓶中反应的方程式
CH3CH2OH
CH2=CH2↑+H2O
| 浓H2SO4 |
| 170℃ |
CH3CH2OH
CH2=CH2↑+H2O
,反应类型| 浓H2SO4 |
| 170℃ |
消去反应
消去反应
;(2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式:
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
;
| ||
(3)为了检验乙烯的生成,试管中应盛放
高锰酸钾溶液(或溴的四氯化碳溶液)
高锰酸钾溶液(或溴的四氯化碳溶液)
,现象为溶液褪色
溶液褪色
;(4)洗瓶中盛放的试剂为
氢氧化钠溶液
氢氧化钠溶液
,作用吸收SO2CO2
吸收SO2CO2
某学习小组同学为了确定盐酸、苯酚、碳酸的酸性强弱,设计了如图3所示的装置图进行实验:
(1)锥形瓶内装某可溶性盐,写出A中反应的离子方程式:
CO32-+2H+=H2O+CO2↑
CO32-+2H+=H2O+CO2↑
;(2)C中的现象为
白色浑浊
白色浑浊
,写出C中反应的化学方程式:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,
C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,
(3)B中的试剂为
饱和碳酸氢钠溶液
饱和碳酸氢钠溶液
,作用吸收CO2中的HCl
吸收CO2中的HCl
. 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH水溶液和5mL 溴乙烷,振荡.
实验操作II:将试管如图固定后,水浴加热.
(1)写出该实验的反应方程式:
CH3CH2Br+NaOH
CH3CH2OH+NaBr
| ||
| △ |
CH3CH2Br+NaOH
CH3CH2OH+NaBr
.
| ||
| △ |
(2)用水浴加热而不直接用酒精灯加热的原因是
使试管受热均匀,减少溴乙烷的损失
使试管受热均匀,减少溴乙烷的损失
.(3)装置中长玻璃管的作用是
冷凝回流挥发的溴乙烷
冷凝回流挥发的溴乙烷
.(4)观察到
溶液分层消失
溶液分层消失
现象时,表明溴乙烷与NaOH溶液已完全反应.(5)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的物质是
乙烯
乙烯
.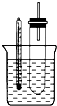 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL溴乙烷,振荡.
实验操作Ⅱ:将试管如图固定后,水浴加热.
(1)试管口安装一长导管的作用是
(2)观察到
(3)鉴定生成物中乙醇的结构,可用的波谱是
(4)检验水解产物中的溴离子的方法是
(5)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验产物,检验的方法是