摘要:19.用足量MnO2与VmL10mol·L-1的盐酸共热制Cl2.在标准状况下.产生2.24LCl2.则V值应为( ) A.V=20 B.V=40 C.40>V>20 D.V>40
网址:http://m.1010jiajiao.com/timu3_id_366851[举报]
实验室用足量MnO2与浓盐酸反应制取氯气,其装置如图1所示:
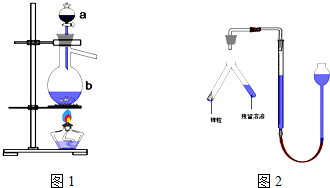
(1)图1中仪器a的名称是: ;仪器b的名称是: ;b中加入碎瓷片的作用是: .
(2)请写出仪器b中发生的反应的离子方程式:
(3)检查装置的气密性之后的操作依次是: 、 、 .(填序号)
A.向烧瓶中加入MnO2粉末
B.加热
C.向烧瓶中加入浓盐酸
(4)该反应会因为盐酸浓度下降而停止.为了测定反应残留液中盐酸的浓度,某探究小组提出下列实验方案:
①甲同学的方案为:与足量AgNO3溶液反应,称量生成沉淀的质量.
②乙同学的方案为:与足量的锌反应,测量生成气体的体积,实验装置如图2所示(夹持装置已略去).使Y形管中的残留溶液与锌粒反应的正确操作是 (“锌粒转移到残留溶液中”或“残留溶液转移到锌粒中”).在正确读取量气管读数时,视线要平视,要注意使漏斗液面与量气管中液面相平,除此外还须注意: .两种方案我认为 (填甲或乙)同学的方案可行.
查看习题详情和答案>>

(1)图1中仪器a的名称是:
(2)请写出仪器b中发生的反应的离子方程式:
(3)检查装置的气密性之后的操作依次是:
A.向烧瓶中加入MnO2粉末
B.加热
C.向烧瓶中加入浓盐酸
(4)该反应会因为盐酸浓度下降而停止.为了测定反应残留液中盐酸的浓度,某探究小组提出下列实验方案:
①甲同学的方案为:与足量AgNO3溶液反应,称量生成沉淀的质量.
②乙同学的方案为:与足量的锌反应,测量生成气体的体积,实验装置如图2所示(夹持装置已略去).使Y形管中的残留溶液与锌粒反应的正确操作是