摘要: 18.在0.1mol·L-1 Na2CO3溶液中.下列关系正确的是 A.c(Na+)=2c(CO32-) B.c(OH-)=2c(H+) C.c(HCO3-)>c(H2CO3) D.c(Na+)<{c(CO32-)+c(HCO3-)}
网址:http://m.1010jiajiao.com/timu3_id_366050[举报]
已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36.常温时下列有关说法正确的是( )
| A、除去工业废水中的Cu2+可以选用FeS作沉淀剂 | B、向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强 | C、因为H2SO4是强酸,所以反应:CuSO4+H2S=CuS↓+H2SO4不能发生 | D、将足量的CuSO4溶解在0.1mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L |
市场上有各种品牌的抗胃酸药,如复方氢氧化铝、盐酸雷尼替丁等.某研究性学习小组为了探究它们的差别及效果进行如下实验:
实验仪器:研钵、250mL烧杯、100mL量筒、电子天平
实验药品:复方氢氧化铝、盐酸雷尼替丁、0.05mol/L盐酸、蒸馏水
实验过程:
实验一:
①称量1.000g研磨后的复方氢氧化铝放入烧杯中,加入75mL蒸馏水搅拌使药品溶解;
②向溶液中缓慢滴入0.05mol/L盐酸,不断搅拌并测量溶液的pH;
③至测量的pH在3.00时,且30s内基本不变停止滴加,记录读数,重复滴定两次;
④将药品换成1.000g盐酸雷尼替丁重复上述步骤.
实验数据如下:
实验二:
①在烧杯中加入0.05mol/L盐酸50mL;
②在溶液中加入1.000g复方氢氧化铝粉末,不断搅拌,计时并同时记录pH读数的变化;
③将复方氢氧化铝粉末换成盐酸雷尼替丁重复上述步骤.
实验数据如下:
试回答下列问题:
(1)完成上述实验还缺少的仪器有 、 .
(2)用盐酸雷尼替丁进行实验二时,0~1.5min内pH减小的原因是: ;实验二不能反映药品发生反应时的实际环境,且实验时间较长,你认为应该如何控制该实验的条件 .
(3)请你根据上述实验,得出合理的实验结论:
① ;② .
查看习题详情和答案>>
实验仪器:研钵、250mL烧杯、100mL量筒、电子天平
实验药品:复方氢氧化铝、盐酸雷尼替丁、0.05mol/L盐酸、蒸馏水
实验过程:
实验一:
①称量1.000g研磨后的复方氢氧化铝放入烧杯中,加入75mL蒸馏水搅拌使药品溶解;
②向溶液中缓慢滴入0.05mol/L盐酸,不断搅拌并测量溶液的pH;
③至测量的pH在3.00时,且30s内基本不变停止滴加,记录读数,重复滴定两次;
④将药品换成1.000g盐酸雷尼替丁重复上述步骤.
实验数据如下:
| 复方氢氧化铝 | 盐酸雷尼替丁 | |||
| 滴定前 | 滴定后 | 滴定前 | 滴定后 | |
| 1 | 0.01 | 79.8 | 0.02 | 18.6 |
| 2 | 0.00 | 79.5 | 0.03 | 19.0 |
| 3 | 0.03 | 80.5 | 0.00 | 18.7 |
①在烧杯中加入0.05mol/L盐酸50mL;
②在溶液中加入1.000g复方氢氧化铝粉末,不断搅拌,计时并同时记录pH读数的变化;
③将复方氢氧化铝粉末换成盐酸雷尼替丁重复上述步骤.
实验数据如下:
| 时间(min) | 0 | 0.5 | 1 | 1.5 | 2 | 2.5 | 3 | 3.5 | 4 | 5 |
| 复方氢氧化铝 | 3.53 | 3.62 | 3.70 | 3.75 | 3.79 | 3.84 | 3.88 | 3.89 | 3.90 | 3.92 |
| 盐酸雷尼替丁 | 1.72 | 1.65 | 1.60 | 1.55 | 1.74 | 1.80 | 1.84 | 1.87 | 1.87 | 1.88 |
| 时间(min) | 10 | 15 | 20 | 25 | 30 | 35 | 40 | |||
| 复方氢氧化铝 | 3.97 | 4.01 | 4.12 | 4.13 | 4.14 | 4.15 | 4.15 | |||
| 盐酸雷尼替丁 | 1.88 | 1.87 | 1.88 |
(1)完成上述实验还缺少的仪器有
(2)用盐酸雷尼替丁进行实验二时,0~1.5min内pH减小的原因是:
(3)请你根据上述实验,得出合理的实验结论:
①
(2010?启东市模拟)联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020
年,单位GDP二氧化碳排放比2005年下降40%~45%.
(1)有效“减碳”的手段之一是节能.下列制氢方法最节能的是
A.电解水制氢:2H2O
2H2↑+O2↑ B.高温使水分解制氢:2H2O
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O
2H2↑+O2↑
D.天然气制氢:CH4+H2O
CO+3H2
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应: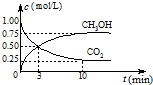
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从3min到10min,v(H2)=
②能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
③下列措施中能使n (CH3OH)/n (CO2)增大的是
A.升高温度B.恒温恒容充入He(g)
C.将H2O(g)从体系中分离 D.恒温恒容再充入1mol CO2和3mol H2
④相同温度下,如果要使氢气的平衡浓度为1mol/L,则起始时应向容器中充入1mol CO2和
(参考数据:
=2.64;
=21.166.计算结果请保留3位有效数字.)
(3)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一.
2CO2(g)+6H2(g)→CH3OCH3(g)+3H2O.有人设想利用二甲醚制作燃料电池,
以KOH溶液做电解质溶液,试写出该电池工作时负极反应的电极反应方程式
查看习题详情和答案>>
年,单位GDP二氧化碳排放比2005年下降40%~45%.
(1)有效“减碳”的手段之一是节能.下列制氢方法最节能的是
C
C
.(填字母序号)A.电解水制氢:2H2O
| ||
| ||
C.太阳光催化分解水制氢:2H2O
| ||
| 太阳光 |
D.天然气制氢:CH4+H2O
| 高温 |
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:

CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从3min到10min,v(H2)=
0.11
0.11
mol/(L?min).②能说明上述反应达到平衡状态的是
D
D
(选填编号).A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
③下列措施中能使n (CH3OH)/n (CO2)增大的是
CD
CD
(选填编号).A.升高温度B.恒温恒容充入He(g)
C.将H2O(g)从体系中分离 D.恒温恒容再充入1mol CO2和3mol H2
④相同温度下,如果要使氢气的平衡浓度为1mol/L,则起始时应向容器中充入1mol CO2和
3.58
3.58
mol H2,平衡时CO2的转化率为86.1%
86.1%
.(参考数据:
| 7 |
| 448 |
(3)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一.
2CO2(g)+6H2(g)→CH3OCH3(g)+3H2O.有人设想利用二甲醚制作燃料电池,
以KOH溶液做电解质溶液,试写出该电池工作时负极反应的电极反应方程式
C2H6O+16OH--12e-═2CO32-+11H2O
C2H6O+16OH--12e-═2CO32-+11H2O
.(1)Na2CO3溶液显
(2)将0.1mol Na2CO3和0.1mol NaHCO3混合后完全溶于水,所得溶液离子浓度由大到小的顺序为
(3)在2支试管里分别加入少量Na2CO3和NaHCO3(各约1g),观察二者外观上的细小差别.分别滴入几滴水,振荡试管,用手触摸试管底部,感觉
实验一
实验二:Na2CO3、NaHCO3饱和溶液分别与盐酸恰好完全反应
请回答:
①通过上述实验可以得出
A.NaHCO3的溶解过程表现为吸热
B.NaHCO3的饱和溶液与盐酸反应表现为吸热
C.Na2CO3的溶解过程表现为放热
D.Na2CO3的饱和溶液与盐酸反应表现为吸热
②结论:NaHCO3固体与稀盐酸反应过程中的能量变化与
查看习题详情和答案>>
碱性
碱性
(填“酸性”、“中性”或“碱性”),原因是(用离子方程式表示)CO32-+H2O HCO3-+OH-
HCO3-+OH-
 HCO3-+OH-
HCO3-+OH-CO32-+H2O HCO3-+OH-
HCO3-+OH-
. HCO3-+OH-
HCO3-+OH-(2)将0.1mol Na2CO3和0.1mol NaHCO3混合后完全溶于水,所得溶液离子浓度由大到小的顺序为
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.(3)在2支试管里分别加入少量Na2CO3和NaHCO3(各约1g),观察二者外观上的细小差别.分别滴入几滴水,振荡试管,用手触摸试管底部,感觉
盛Na2CO3溶液的试管底部发热,盛NaHCO3溶液的试管底部感受不到热量变化
盛Na2CO3溶液的试管底部发热,盛NaHCO3溶液的试管底部感受不到热量变化
.为进一步研究NaHCO3、Na2CO3和同浓度稀盐酸反应过程中的热效应,进行了如下实验(数据为三次取平均值):实验一
| 试剂1 | 试剂2温度(℃) | 溶解后温度(℃) |
| 0.5g NaHCO3固体 | 10mL水 19.0 | 18.4 |
| 0.5 g Na2CO3固体 | 10mL水 19.0 | 25.5 |
| 试剂1/温度(℃) | 试剂2/温度(℃) | 恰好反应后温度(℃) |
| 含0.5g NaHCO3固体的饱和溶液/19.0 | 6mL稀盐酸/19.0 | 18.3 |
| 含0.5 g Na2CO3固体的饱和溶液/19.0 | 9mL稀盐酸/19.0 | 22.1 |
①通过上述实验可以得出
A、B、C
A、B、C
(填字母编号);A.NaHCO3的溶解过程表现为吸热
B.NaHCO3的饱和溶液与盐酸反应表现为吸热
C.Na2CO3的溶解过程表现为放热
D.Na2CO3的饱和溶液与盐酸反应表现为吸热
②结论:NaHCO3固体与稀盐酸反应过程中的能量变化与
NaHCO3的溶解过程、NaHCO3溶液与盐酸反应的热效应
NaHCO3的溶解过程、NaHCO3溶液与盐酸反应的热效应
有关.