网址:http://m.1010jiajiao.com/timu3_id_364785[举报]
76.8mg铜和适量浓硝酸反应,铜全部溶解后,如果NO3-离子减少2×10-3 mol,则溶液中H+同时下降( )。
A.2×10-3 mol B.3.2×10-3 mol
C.4.4×10-3 mol D. 4×10-3 mol
查看习题详情和答案>>已知:
①NO+NO2+2OH-=2NO2-+H2O
②气体液化温度 NO221℃NO-152℃
请回答:
(1)写出铜与浓硝酸反应的化学反应方程式
(2)装置B的作用是
(3)写出装置的连接顺序(填字母),A接B接
(4)实验开始前要先打开A装置中的活塞K1,持续通一段时间氮气后再关闭活塞K1,目的是
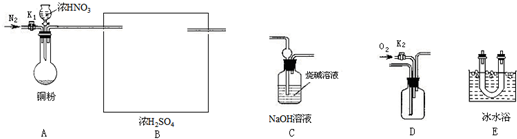
(5)如果O2过量,则装置C中发生反应的离子方程式是
(6)若铜粉中混入了少量银,已知铜粉质量为a g,反应后固体完全溶解,要测定铜粉中铜的质量分数,只需利用A装置中反应后的溶液进行简单的实验操作,就可以达到实验目的.试简述实验方案
(1)参与反应的HNO3的物质的量.
(2)生成的混合气体中NO的体积.
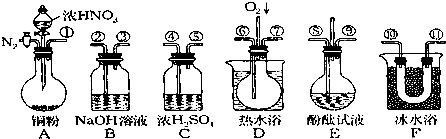
已知:
①NO+NO2+OH-→2NO2-+H2O;
②气体液化温度:NO2:21℃,NO:-152℃.试回答:
(1)选择必要的仪器,则仪器的连接顺序(按左→右连接,填各接口的编号)为:
(3)确认气体中含有NO的现象是
(4)装置F的作用是
(5)若O2过量,B中反应的化学方程式为
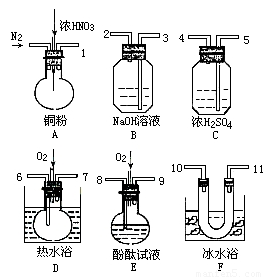
用下列仪器、药品验证由铜和适量硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制)。
已知:①
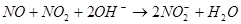 ② 气体液化温度:NO2 21℃, NO -152℃
② 气体液化温度:NO2 21℃, NO -152℃
试回答:
(1)写出装置A中发生反应的化学方程式_____ 。
(2)仪器的连接顺序(按左→右连接,填各接口的编号)为____
。在填加药
品前应先进行的操作是 。
(3)反应前先通入N2,目的是______ ;
(4)确认气体中含NO的现象是________ 。
(5)装置B、F的作用是 _______ 。
(6)若从A出来的混合气体中NO2、NO的体积分别为V1mL、V2mL,若最终氮的氧化物完全被溶液吸收,装置中至少需要充入氧气的体积为: (相同状态下)。
查看习题详情和答案>>