摘要:X.Y.Z.W四种短周期元素.若X的阳离子与Y的阴离子具有相同的电子层结构.W的阳离子氧化性强于等电荷的X阳离子的氧化性.Z的阴离子半径大于等电荷的Y的阴离子半径.且Z离子所带电荷数的绝对值是W离子的两倍.W离子与Z离子的电子层相差两层.试推断这四种元素X .Y .Z .W .
网址:http://m.1010jiajiao.com/timu3_id_364482[举报]
X、Y、Z、W四种短周期元素,原子序数依次增大.X原子的最外层上p电子数与s电子数相等;Y有两种常见的同素异形体,其中一种是很好的脱色剂和消毒剂;Z、W原子最外层电子数之和是X最外层电子数的2倍;这四种元素的电子层数之和为10.据此推断下列说法不正确的是( )
查看习题详情和答案>>
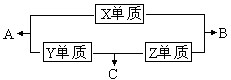 X、Y、Z、W四种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、W四种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:已知一个B分子中含有的Z元素的原子个数比一个C分子中少一个.而W的单质在常温常压下为固体,并且W元素是形成化合物种类最多的元素.请回答下列问题:
(1)元素X在周期表中的位置
第2周期第ⅥA族
第2周期第ⅥA族
,Y单质的电子式

(2)化合物C在一定条件下生成化合物A的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(3)常温下,将C通入元素Y的最高价氧化物的水化物的水溶液中,恰好完全反应时溶液呈
酸
酸
性(填“酸”、“碱”、“中”);此时溶液中离子浓度由大到小的顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-)
c(NO3-)>c(NH4+)>c(H+)>c(OH-)
.(4)由X、Y、Z、W四种元素组成的无机酸酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为
NH4++HCO3-+2OH-
NH3↑+2H2O+CO32-
| ||
NH4++HCO3-+2OH-
NH3↑+2H2O+CO32-
.
| ||
(5)由X、Z、W三种元素可以形成化合物W2Z6X,其蒸汽通过灼热的氧化铜,黑色的氧化铜会逐渐变红,则该反应的化学方程式为
CH3CH2OH+CuO
CH2CHO+Cu+H2O
| △ |
CH3CH2OH+CuO
CH2CHO+Cu+H2O
.| △ |
X、Y、Z、W四种短周期元素,若符合下面的要求,则这四种元素的原子序数由大到小的顺序为( )
①X的阳离子与Y的阴离子具有相同的电子层结构
②W的阳离子的氧化性强于同主族带等电荷数的X的阳离子的氧化性 ③Z的阴离子半径大于同主族带等电荷数的Y的阴离子半径
A.W>Y>X>Z B.Z>Y>W>X
C.X>Y>Z>W D.Z>X>Y>W
查看习题详情和答案>>