摘要:15.2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂.工业上冶炼钼的化学原理为 ①2MoS2+7O2 2MoO3+4SO2, ②MoO3+2NH3·H2O====(NH4)2MoO4+H2O, ③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl, ④H2MoO4MoO3+H2O; ⑤用还原剂将MoO3还原成金属钼. 则下列说法正确的是 A.MoS2煅烧产生的尾气可直接排空 B.MoO3是金属氧化物.也是碱性氧化物 C.H2MoO4是一种强酸 D.利用H2.CO和铝分别还原等量的MoO3.所消耗还原剂的物质的量之比为3∶3∶2 16.铁粉和铜粉的均匀混合物.平均分成四等份.分别加入同浓度的稀硝酸.充分反应.在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO): 编号 ① ② ③ ④ 稀硝酸体积/mL 100 200 300 400 剩余金属/g 18.0 9.6 0 0 NO体积/mL 2240 4480 6720 V 下列计算结果正确的是( ) A.①中溶解了5.6gFe B.硝酸的浓度为4mol/L C.②中溶解了9.6gCu D.④中V=8960 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu3_id_364396[举报]
2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:?
①2MoS2+7O2![]() 2MoO3+4SO2
2MoO3+4SO2
②MoO3+2NH3·H2O![]() (NH4)
(NH4)
③(NH4)![]() H
H
④H![]() MoO3+H2O
MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。则下列说法中正确的是( )?
A.MoS2煅烧产生的尾气不可直接排到空气中?
B.MoO3是金属氧化物,也是碱性氧化物?
C.H2MoO4是一种强酸?
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
查看习题详情和答案>>
2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为
①2MoS2+7O2![]() 2MoO3+4SO2;
2MoO3+4SO2;
②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;
④H2MoO4![]() MoO3+H2O;
MoO3+H2O;
⑤用还原剂MoO3还原成金属钼。
则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3不溶于氢氧化钠溶液
C.H2MoO4是一种强酸
D.利用H2、CO和铝分别还原等量的MoO3,消耗还原剂的物质的量之比为3∶3∶2
查看习题详情和答案>>
2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:①2MoS2+7O2 2MoO3+4SO2;②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;④H2MoO4
2MoO3+4SO2;②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;④H2MoO4 MoO3+H2O;⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是
MoO3+H2O;⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是
A.MoS2燃烧产生的尾气可直接排空
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一种强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
查看习题详情和答案>>
2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为①2MoS2+7O2 2MoO3+4SO2;②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;④H2MoO4
2MoO3+4SO2;②MoO3+2NH3·H2O====(NH4)2MoO4+H2O;③(NH4)2MoO4+2HCl====H2MoO4↓+2NH4Cl;④H2MoO4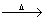 MoO3+H2O;⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是( )
MoO3+H2O;⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是( )
A.MoS2煅烧产生的尾气可直接排入空气中
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一种强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
查看习题详情和答案>>