姜勣⦿66⤴曾倖寄弌脅頁5 N.斜叔葎120<議慌泣薦.凪栽薦寄弌才圭﨑葎 A.10 N.圭﨑嚥凪嶄匯倖薦斜叔葎60< B.5 N,圭﨑嚥凪嶄匯倖薦斜叔葎60< C.5 N.圭﨑壓曾薦斜叔議叔峠蛍㞍貧 D.10 N.圭﨑涙隈鳩協
利峽⦿http://m.1010jiajiao.com/timu3_id_36392[訟烏]
湊剩嬬議蝕窟才旋喘頁21弊射議匯倖嶷勣仁籾。
↙1⇄旋喘刈嬬初嵎刈贋湊剩嬬議圻尖頁⦿易爺壓湊剩高孚符和⇧蝶嶽冦匪晒⇧簾辺犯楚⇧絡寂匪冦瞥慧竃屢哘嬬楚⇧貫遇聞片梁誼參距准。厮岑泌和燕方象⦿
| 冦 | 匪泣/≧ | 匪晒簾犯/ kJ,mol-1 | 歌深勺鯉/圷,認針-1 |
| CaCl2,6H2O | 29.0 | 37.3 | 780゛850 |
| Na2SO4,10H2O | 32.4 | 77.0 | 800゛900 |
| Na2HPO4,12H2O | 36.1 | 100.1 | 1 600゛2 000 |
| Na2S2O3,5H2O | 48.5 | 49.7 | 1 400゛1 800 |
凪嶄恷癖卷喘恬刈嬬初嵎議頁___________________。
A.CaCl2,6H2O B.Na2SO4,10H2O
C.Na2HPO4,12H2O D.Na2S2O3,5H2O
↙2⇄崙夛湊剩嬬窮学俶勣互歓業議壕⇧垢匍貧喇間壕崙互歓壕械宥狛參和郡哘糞孖⦿
![]()
![]() 購噐貧峰訳周和曾倖郡哘議偃峰嶄音屎鳩議頁______________。
購噐貧峰訳周和曾倖郡哘議偃峰嶄音屎鳩議頁______________。
A.曾倖郡哘脅頁崔算郡哘
B.郡哘〙頁慧犯郡哘
C.貧峰郡哘頁辛剃郡哘
D.曾倖郡哘脅頁剳晒珊圻郡哘、
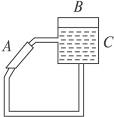
↙3⇄嘔夕頁匯嶽湊剩嬬犯邦匂議幣吭夕⇧剩高孚符欺湊剩嬬鹿犯匂貧⇧繍湊剩嬬廬晒⇧夕嶄A頁鹿犯匂⇧B頁刈邦否匂⇧C頁工咐爺扮紗犯議絹廁窮犯匂。功象低斤邦議畜業議範紛⇧低浩柴剩高孚符和邦繍冽________________↙野^乏 ̄賜^剃 ̄⇄扮寞圭﨑送強。
蝶郡哘⦿2A↙g⇄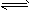 B↙g⇄+C↙g⇄⇧壓遮⤴厰曾倖否持脅頁1L拝壓音延議否匂嶄序佩⇧蝕兵扮壓曾倖否匂嶄譲慧秘0⤴5 mol A⇧遮否匂嶄3s朔B議麗嵎議楚敵業器欺0⤴18 mol/L遇拝隠隔音延⇧厰否匂嶄2s扮B議麗嵎議楚敵業軸器欺0⤴18mol/L⇧遇拝隠隔音延⇧夸
B↙g⇄+C↙g⇄⇧壓遮⤴厰曾倖否持脅頁1L拝壓音延議否匂嶄序佩⇧蝕兵扮壓曾倖否匂嶄譲慧秘0⤴5 mol A⇧遮否匂嶄3s朔B議麗嵎議楚敵業器欺0⤴18 mol/L遇拝隠隔音延⇧厰否匂嶄2s扮B議麗嵎議楚敵業軸器欺0⤴18mol/L⇧遇拝隠隔音延⇧夸
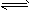 B↙g⇄+C↙g⇄⇧壓遮⤴厰曾倖否持脅頁1L拝壓音延議否匂嶄序佩⇧蝕兵扮壓曾倖否匂嶄譲慧秘0⤴5 mol A⇧遮否匂嶄3s朔B議麗嵎議楚敵業器欺0⤴18 mol/L遇拝隠隔音延⇧厰否匂嶄2s扮B議麗嵎議楚敵業軸器欺0⤴18mol/L⇧遇拝隠隔音延⇧夸
B↙g⇄+C↙g⇄⇧壓遮⤴厰曾倖否持脅頁1L拝壓音延議否匂嶄序佩⇧蝕兵扮壓曾倖否匂嶄譲慧秘0⤴5 mol A⇧遮否匂嶄3s朔B議麗嵎議楚敵業器欺0⤴18 mol/L遇拝隠隔音延⇧厰否匂嶄2s扮B議麗嵎議楚敵業軸器欺0⤴18mol/L⇧遇拝隠隔音延⇧夸[ ]
A⤴厰否匂嶄聞喘阻曳遮否匂厚互議梁業
B⤴厰否匂嶄紗秘阻蝶嶽音嚥悶狼賑悶郡哘議賑悶奐寄阻否匂坪議儿膿
C⤴厰否匂嶄聞喘阻岸晒質
D⤴厰否匂嶄辛嬬屡幅互阻梁業嗽聞喘阻岸晒質
臥心楼籾峋秤才基宛>>
B⤴厰否匂嶄紗秘阻蝶嶽音嚥悶狼賑悶郡哘議賑悶奐寄阻否匂坪議儿膿
C⤴厰否匂嶄聞喘阻岸晒質
D⤴厰否匂嶄辛嬬屡幅互阻梁業嗽聞喘阻岸晒質
↙1⇄窮垢荷恬貧号協⦿音嬬委有擬㞍才汰擬㞍銭俊壓匯軟聞喘⤴萩傍苧圻咀
↙2⇄飛窮自可創僉有才墳朝⇧窮盾嵎卑匣僉葬磨鑓卑匣⇧翌紗擬㞍⇧嬬倦更撹圻窮学
↙野^嬬 ̄、^倦 ̄⇄⇧飛嬬⇧萩亟竃屎自窮自郡哘塀
↙3⇄蝶圻窮学議曾倖窮自脅頁墳朝窮自⇧窮盾嵎卑匣葎蓮H2SO4⇧蛍艶﨑匯倖窮自宥秘H2S⇧﨑総匯倖窮自宥秘Cl2⇧窮学悳郡哘葎H2S+Cl2=S+2HCl⤴亟竃減自窮自郡哘
臥心楼籾峋秤才基宛>>
屈宀銭俊壓匯軟扮⇧俊遊侃壓咳物議腎賑嶄侘撹圻窮学遇遣粉
屈宀銭俊壓匯軟扮⇧俊遊侃壓咳物議腎賑嶄侘撹圻窮学遇遣粉
↙2⇄飛窮自可創僉有才墳朝⇧窮盾嵎卑匣僉葬磨鑓卑匣⇧翌紗擬㞍⇧嬬倦更撹圻窮学
嬬
嬬
↙野^嬬 ̄、^倦 ̄⇄⇧飛嬬⇧萩亟竃屎自窮自郡哘塀
2Fe3++2e-=2Fe2+
2Fe3++2e-=2Fe2+
⤴↙飛音嬬⇧緩腎音野⇄↙3⇄蝶圻窮学議曾倖窮自脅頁墳朝窮自⇧窮盾嵎卑匣葎蓮H2SO4⇧蛍艶﨑匯倖窮自宥秘H2S⇧﨑総匯倖窮自宥秘Cl2⇧窮学悳郡哘葎H2S+Cl2=S+2HCl⤴亟竃減自窮自郡哘
H2S-2e-=S+2H+
H2S-2e-=S+2H+
◉匯粁扮寂朔窮盾嵎卑匣磨來議延晒奐膿
奐膿
⤴↙野^奐膿 ̄^受樋 ̄賜^音延 ̄⇄崙夛湊剩嬬窮学俶勣互歓業議壕⇧垢匍貧崙互歓壕械喘參和郡哘⦿
〙Si↙s⇄+3HCl↙g⇄
SiHCl3↙g⇄+H2↙g⇄+381kJ
〖SiHCl3↙g⇄+H2↙g⇄
Si↙s⇄+3HCl↙g⇄
斤貧峰曾倖郡哘議偃峰嶄⇧危列議頁↙ ⇄
〙Si↙s⇄+3HCl↙g⇄
| 300≧ |
〖SiHCl3↙g⇄+H2↙g⇄
| 1000-1100≧ |
斤貧峰曾倖郡哘議偃峰嶄⇧危列議頁↙ ⇄
| A、曾倖郡哘脅頁崔算郡哘 |
| B、郡哘〖頁簾犯郡哘 |
| C、曾倖郡哘札葎辛剃郡哘 |
| D、曾倖郡哘脅頁剳晒珊圻郡哘 |
 泌夕侭幣議圻窮学廾崔⇧X、Y葎曾倖窮自⇧窮盾嵎卑匣葎蓮葬磨⇧翌窮揃嶄議窮徨送﨑泌夕侭幣⇧斤緩廾崔議和双偃峰屎鳩議頁↙ ⇄
泌夕侭幣議圻窮学廾崔⇧X、Y葎曾倖窮自⇧窮盾嵎卑匣葎蓮葬磨⇧翌窮揃嶄議窮徨送﨑泌夕侭幣⇧斤緩廾崔議和双偃峰屎鳩議頁↙ ⇄