摘要:物体在斜面上保持静止状态.下列说法中正确的是 ①重力可分解为沿斜面向下的力和对斜面的压力 ②重力沿斜面向下的分力与斜面对物体的静摩擦力大小是相等的 ③物体对斜面的压力与斜面对物体的支持力是一对平衡力 ④重力垂直于斜面方向的分力与斜面对物体的支持力大小是相等的 A.①② B.①③ C.②③ D.②④
网址:http://m.1010jiajiao.com/timu3_id_36386[举报]
 17.
17.
(如东启东期中联考14分)如图所示,可视为质点的三物块A、B、C放在倾角为300、长L=2m的固定斜面上,物块与斜面间的动摩擦因数μ=![]() ,A与B紧靠在一起,C紧靠在固定挡板上,三物块的质量分别为mA=0.80kg、mB=0.64kg、mC=0.50kg,其中A不带电,B、C的带电量分别为qB=+4.0×10-5C、qC=+2.0×10-5C且保持不变,开始时三个物块均能保持静止且与斜面间均无摩擦力作用.如果选定两点电荷在相距无穷远处的电势能为0,则相距为r时,两点电荷具有的电势能可表示为
,A与B紧靠在一起,C紧靠在固定挡板上,三物块的质量分别为mA=0.80kg、mB=0.64kg、mC=0.50kg,其中A不带电,B、C的带电量分别为qB=+4.0×10-5C、qC=+2.0×10-5C且保持不变,开始时三个物块均能保持静止且与斜面间均无摩擦力作用.如果选定两点电荷在相距无穷远处的电势能为0,则相距为r时,两点电荷具有的电势能可表示为![]() .现给A施加一平行于斜面向上的力F,使A在斜面上作加速度a=1.5m/s2的匀加速直线运动,经过时间t0,力F变为恒力,当A运动到斜面顶端时撤去力F.已知静电力常量k=9.0×109N?m2/C2,g=10m/s2.求:
.现给A施加一平行于斜面向上的力F,使A在斜面上作加速度a=1.5m/s2的匀加速直线运动,经过时间t0,力F变为恒力,当A运动到斜面顶端时撤去力F.已知静电力常量k=9.0×109N?m2/C2,g=10m/s2.求:
(1)未施加力F时物块B、C间的距离;
(2)t0时间内A上滑的距离;
(3)t0时间内库仑力做的功;
(4)力F对A物块做的总功.
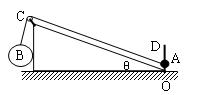
查看习题详情和答案>>如图所示,整个装置处于静止状态,A、B两球由一根跨过定滑轮的轻绳相连接,A为一带孔小球,穿在光滑固定的竖直杆OD上,且A球与斜面不接触,B与斜面体的接触面光滑,C处滑轮摩擦不计,C、B之间的绳与竖直方向成300角,C、A之间的绳与斜面平行,斜面倾角θ为300,则A、B两球的质量比为 ( )
A.![]() B.1
B.1
C.![]() D.
D.![]()
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g )+2H2(g)?CH3OH(g ).图1表示反应过程中能量的变化情况:图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g )的浓度随时间的变化情况.
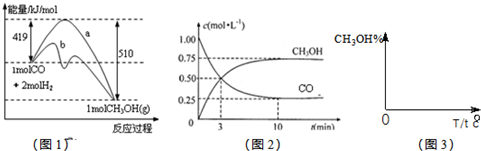
请回答下列问题.
(1)在“图1”中,曲线
(2)下列说法正确的是
a.起始充入的CO为2mol
b.增大CO的浓度,CO的转化率增大
c.容器中压强恒定时,说明反应已达平衡状态
d.保持温度和密闭容器的容积不变,再充入1mol CO和2mol H2,再次达到平衡时n(CH3OH)/n(CO)的值会变小
(3)从反应开始到达平衡,v(H2)=
(4)请在“图3”中画出平衡时甲醇的百分含量(纵坐标)随温度(横坐标)的变化曲线,
要求画出压强不同的两条曲线(在曲线上标出p1、p2,且p1<p2)
 .
.
查看习题详情和答案>>

请回答下列问题.
(1)在“图1”中,曲线
b
b
(填“a”或“b”)表示使用了催化剂;该反应属于放热
放热
(填“吸热”或“放热”)反应.(2)下列说法正确的是
ac
ac
(填字母序号).a.起始充入的CO为2mol
b.增大CO的浓度,CO的转化率增大
c.容器中压强恒定时,说明反应已达平衡状态
d.保持温度和密闭容器的容积不变,再充入1mol CO和2mol H2,再次达到平衡时n(CH3OH)/n(CO)的值会变小
(3)从反应开始到达平衡,v(H2)=
0.15
0.15
;该温度下CO (g)+2H2(g)?CH3OH(g)的化学平衡常数为12
12
.若保持其他条件不变,将反应体系升温,则该反应的化学平衡常数减小
减小
(填“增大”、“减小”或“不变”).(4)请在“图3”中画出平衡时甲醇的百分含量(纵坐标)随温度(横坐标)的变化曲线,
要求画出压强不同的两条曲线(在曲线上标出p1、p2,且p1<p2)


金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s)+3H2 (g)
W (s)+3H2O (g)
请回答下列问题:
(1)在一定温度下进行上述反应,若反应容器的容积为0.5L,2min后达到平衡,测得固体的质量减少了4.80g,则H2的平均反应速率
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为
(3)一定温度下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是
A.混合气体的总压强保持不变 B.v正(H20)=v正(H2)
C.混合气体的密度保持不变 D. 混合气体的平均式量保持不变
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s)+2I2 (g)
WI4 (g).下列说法正确的有
A.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.灯管内的I2可循环使用.
查看习题详情和答案>>
WO3 (s)+3H2 (g)
| 高温 |
请回答下列问题:
(1)在一定温度下进行上述反应,若反应容器的容积为0.5L,2min后达到平衡,测得固体的质量减少了4.80g,则H2的平均反应速率
0.3 mol/(L?min)
0.3 mol/(L?min)
;该反应的平衡常数表达式K=| c3(H2O) |
| c3(H2) |
| c3(H2O) |
| c3(H2) |
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为
60%
60%
;随温度的升高,H2与水蒸气的体积比减小,则该反应为正反应吸热
正反应吸热
(填“吸热”或“放热”) 反应.(3)一定温度下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是
CD
CD
.A.混合气体的总压强保持不变 B.v正(H20)=v正(H2)
C.混合气体的密度保持不变 D. 混合气体的平均式量保持不变
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s)+2I2 (g)
| 1400℃ |
| 约3000℃ |
BD
BD
.A.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.灯管内的I2可循环使用.
自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产.请回答下列问题:
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
写出氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式: .
(2)在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol?L-1和b mol?L-1,反应为:N2+3H2?2NH3,氨气的浓度随时间变化如图1所示.在10min时采取的措施是 ,点A的平衡常数K (填“<”、“>”或“=”)B点的平衡常数.

(3)若合成塔内生成17g氨气放出45.5kJ热量,在图2坐标上画出该合成氨反应过程中能量随时间的变化示意图.
(4)在一定体积的恒容密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g),其化学平衡常数K与温度t的关系如下表:
①比较K1、K2的大小:K1 K2(填“>”、“=”或“<”).
②判断该反应达到化学平衡状态的依据是 (填序号).
A.2v正(H2)(正)=3v逆(NH3) B.v正(N2)=3v逆(H2)
C.容器内压强保持不变 D.混合气体的密度保持不变
(5)在一定温度和催化剂下,将6.4mol H2和2.4molN2混合于一个容积为4L的密闭容器中发生反应,在3min末时反应恰好达平衡,此时生成了1.6mol NH3.计算该条件下的平衡常数(写出计算过程). .
查看习题详情和答案>>
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
写出氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式:
(2)在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol?L-1和b mol?L-1,反应为:N2+3H2?2NH3,氨气的浓度随时间变化如图1所示.在10min时采取的措施是

(3)若合成塔内生成17g氨气放出45.5kJ热量,在图2坐标上画出该合成氨反应过程中能量随时间的变化示意图.
(4)在一定体积的恒容密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g),其化学平衡常数K与温度t的关系如下表:
| t/K | 298 | 398 | 498 | … |
| K | 4.1×106 | K1 | K2 | … |
②判断该反应达到化学平衡状态的依据是
A.2v正(H2)(正)=3v逆(NH3) B.v正(N2)=3v逆(H2)
C.容器内压强保持不变 D.混合气体的密度保持不变
(5)在一定温度和催化剂下,将6.4mol H2和2.4molN2混合于一个容积为4L的密闭容器中发生反应,在3min末时反应恰好达平衡,此时生成了1.6mol NH3.计算该条件下的平衡常数(写出计算过程).