摘要:8.如图.曲线 a表示一定条件下.可逆反应 X + W(s); △H<0的反应过程.若欲使a曲线变为b曲线.可采取 的措施是 ( ) A.加入催化剂 B.增大Y的浓度 C.降低温度 D.减小反应体系压强
网址:http://m.1010jiajiao.com/timu3_id_362687[举报]
如图,曲线a表示一定条件下,可逆反应X(g) + Y(g) 2Z(g) +W(s),正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是
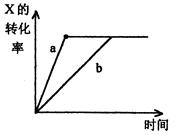
| A.减小Y的浓度 |
| B.增大Y的浓度 |
| C.降低温度 |
| D.减小反应体系的压强 |
如图,曲线a表示一定条件下,可逆反应X(g) + Y(g) 2Z(g) +W(s),正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是

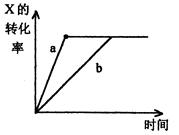
A.减小Y的浓度
B.增大Y的浓度
C.降低温度
D.减小反应体系的压强
查看习题详情和答案>>
如图,曲线a表示一定条件下,可逆反应X(g) + Y(g) 2Z(g) +W(s),正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是

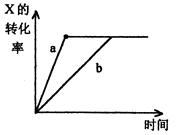


| A.减小Y的浓度 |
| B.增大Y的浓度 |
| C.降低温度 |
| D.减小反应体系的压强 |
如图,曲线a表示一定条件下,可逆反应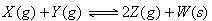 ,正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是
,正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是
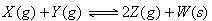 ,正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是
,正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是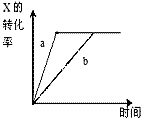
[ ]
A.加入催化剂
B.增大Y的浓度
C.降低温度
D.减小反应体系的压强
查看习题详情和答案>>
B.增大Y的浓度
C.降低温度
D.减小反应体系的压强
 一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)
一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)回答下列问题:
(1)若降低温度,该反应的化学平衡常数
增大
增大
.(填“增大”“减小”或“不变”)(2)该反应处于平衡状态的时间段为
15-20min、25-30min
15-20min、25-30min
.(3)反应进行至20min时,曲线发生变化的原因是
增大氧气的浓度
增大氧气的浓度
(用文字表达).10min到15min的曲线变化的原因可能是a、b
a、b
(填写编号).a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
(4)维持容器体积不变,向该反应的平衡体系中充入氮气,则平衡
不
不
( 填“向左”或“向右”或“不”)移动;维持容器体积不变,向该反应的平衡体系中移走部分混合气体,则平衡向左
向左
( 填“向左”或“向右”或“不”) 移动.