摘要:将KCl和CrCl3两种固体混合.熔烧.可制得化合物X.将1.892gX中的铬元素氧化为Cr2O2-7.则Cr2O2-7可从过量的KI溶液中氧化出2.667g单质碘.反应的 离子方程式为Cr2O2-7+6I-+14H+=2Cr3++3I2+7H2O.现取溶有1. 82 9gX溶液.向其中加入过量的硝酸银溶液.可得4.52g白色沉淀.表示X组成的化学式为( ) (A)K2Cr2Cl7 (B)K3Cr2=Cl5 (C)K3Cr2Cl9 (D)K3Cr2Cl4
网址:http://m.1010jiajiao.com/timu3_id_362583[举报]
将KCl和CrCl3两种固体混合物共熔,得化合物X.X由K、Cr、Cl三种元素组成.将1.892gX中的铬元素全部氧化成Cr2O72-,后者可以从过量的KI溶液中氧化出2.667g碘单质(Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O).向溶有1.892gX的溶液中加入过量AgNO3溶液,可得到4.52g AgCl沉淀.则X的化学式为( )
查看习题详情和答案>>
将KCl和CrCl3两种固体混合物共熔制得化合物X,X由K、Cl、Cr元素组成。将1.892 g X中Cr元素全部氧化成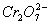 ,
,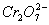 可从过量的KI中氧化出
可从过量的KI中氧化出2.667 g I2,反应的离子方程式是: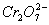 +6I-+14H+====2Cr3++3I2+7H2O,如果取溶有
+6I-+14H+====2Cr3++3I2+7H2O,如果取溶有1.892 g X的溶液,加入过量的AgNO3,可得4.520 g AgCl沉淀,则表示X组成的化学式为
A.K3Cr2Cl9 B.K3Cr2Cl
将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X。将5.405gX中Cr元素全部氧化成Cr2O72-,酸性的Cr2O72-可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O72-被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。(1)写出Cr2O72-与I-反应的离子方程式
(2)通过计算得出X的化学式
查看习题详情和答案>>