摘要:16.下列烧杯中均盛有0.1mol/L的硫酸.锌片腐蚀最快的是
网址:http://m.1010jiajiao.com/timu3_id_360909[举报]
Ⅰ.如图1装置,用离子交换膜法电解饱和食盐水制烧碱.若X电极材料为金属钛网(表面有氧化物涂层),Y电极材料为碳钢网.阳离子交换膜只允许阳离子通过,而阻止阴离子和气体通过.分别收集两极产生的气体并通入淀粉KI溶液中.请回答下列问题:
(1)能使淀粉KI溶液变蓝的是
(2)其阳极的电极反应式为
Ⅱ.如图2所示,甲、乙是两个电化学实验装置.

(1)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为
②电解一段时间后,若要使乙装置中溶液恢复到电解前的状态,可向溶液中加入
(2)起初,若乙装置中盛有含0.5mol NaCl和0.1mol CuSO4的混合溶液.电解一段时间后,当有0.4mole-发生转移时,阴极产生气体
查看习题详情和答案>>
(1)能使淀粉KI溶液变蓝的是
a
a
(填“a”或“b”)气体;(2)其阳极的电极反应式为
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
,阴极的电极反应式为2H++2e=H2↑(或2H2O+2e=H2↑+2OH-)
2H++2e=H2↑(或2H2O+2e=H2↑+2OH-)
;Ⅱ.如图2所示,甲、乙是两个电化学实验装置.

(1)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为
Fe-2e-═Fe2+
Fe-2e-═Fe2+
;②电解一段时间后,若要使乙装置中溶液恢复到电解前的状态,可向溶液中加入
CuO
CuO
;(填写物质的化学式).(2)起初,若乙装置中盛有含0.5mol NaCl和0.1mol CuSO4的混合溶液.电解一段时间后,当有0.4mole-发生转移时,阴极产生气体
0.1
0.1
mol.Ⅰ.如图1装置,用离子交换膜法电解饱和食盐水制烧碱.若X电极材料为金属钛网(表面有氧化物涂层),Y电极材料为碳钢网.阳离子交换膜只允许阳离子通过,而阻止阴离子和气体通过.分别收集两极产生的气体并通入淀粉KI溶液中.请回答下列问题:
(1)能使淀粉KI溶液变蓝的是______(填“a”或“b”)气体;
(2)其阳极的电极反应式为______,阴极的电极反应式为______;
Ⅱ.如图2所示,甲、乙是两个电化学实验装置.
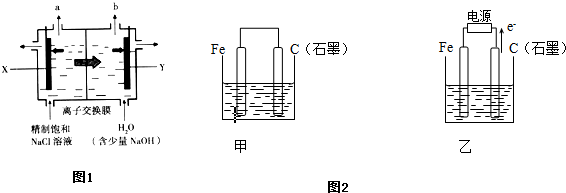
(1)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为______;
②电解一段时间后,若要使乙装置中溶液恢复到电解前的状态,可向溶液中加入______;(填写物质的化学式).
(2)起初,若乙装置中盛有含0.5mol NaCl和0.1mol CuSO4的混合溶液.电解一段时间后,当有0.4mole-发生转移时,阴极产生气体______mol.
查看习题详情和答案>>
(1)能使淀粉KI溶液变蓝的是______(填“a”或“b”)气体;
(2)其阳极的电极反应式为______,阴极的电极反应式为______;
Ⅱ.如图2所示,甲、乙是两个电化学实验装置.

(1)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为______;
②电解一段时间后,若要使乙装置中溶液恢复到电解前的状态,可向溶液中加入______;(填写物质的化学式).
(2)起初,若乙装置中盛有含0.5mol NaCl和0.1mol CuSO4的混合溶液.电解一段时间后,当有0.4mole-发生转移时,阴极产生气体______mol.
Ⅰ.如图1装置,用离子交换膜法电解饱和食盐水制烧碱.若X电极材料为金属钛网(表面有氧化物涂层),Y电极材料为碳钢网.阳离子交换膜只允许阳离子通过,而阻止阴离子和气体通过.分别收集两极产生的气体并通入淀粉KI溶液中.请回答下列问题:
(1)能使淀粉KI溶液变蓝的是 (填“a”或“b”)气体;
(2)其阳极的电极反应式为 ,阴极的电极反应式为 ;
Ⅱ.如图2所示,甲、乙是两个电化学实验装置.
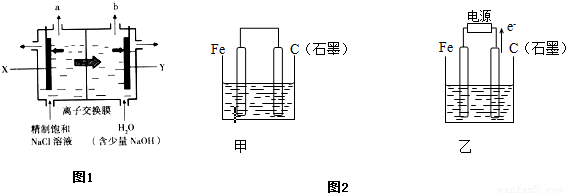
(1)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为 ;
②电解一段时间后,若要使乙装置中溶液恢复到电解前的状态,可向溶液中加入 ;(填写物质的化学式).
(2)起初,若乙装置中盛有含0.5mol NaCl和0.1mol CuSO4的混合溶液.电解一段时间后,当有0.4mole-发生转移时,阴极产生气体 mol. 查看习题详情和答案>>
(1)能使淀粉KI溶液变蓝的是 (填“a”或“b”)气体;
(2)其阳极的电极反应式为 ,阴极的电极反应式为 ;
Ⅱ.如图2所示,甲、乙是两个电化学实验装置.

(1)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为 ;
②电解一段时间后,若要使乙装置中溶液恢复到电解前的状态,可向溶液中加入 ;(填写物质的化学式).
(2)起初,若乙装置中盛有含0.5mol NaCl和0.1mol CuSO4的混合溶液.电解一段时间后,当有0.4mole-发生转移时,阴极产生气体 mol. 查看习题详情和答案>>
高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=akJmol-1
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJmol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJmol-1
则a=
(2)冶炼铁反应的平衡常数表达式K=
,温度升高后,K值
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
①甲容器中CO的平衡转化率为
②下列说法正确的是
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2:3
d.增加Fe2O3可以提高CO的转化率
(4)采取一定措施可防止钢铁腐蚀.下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液.
①在a~c装置中,能保护铁的是
②若用d装置保护铁,X极的电极材料应是
查看习题详情和答案>>
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=akJmol-1
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJmol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJmol-1
则a=
-28.5
-28.5
kJ mol-1.(2)冶炼铁反应的平衡常数表达式K=
| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c3(CO) |
减小
减小
(填“增大”、“不变”或“减小”)(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
60%
60%
.②下列说法正确的是
ac
ac
(填字母).a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2:3
d.增加Fe2O3可以提高CO的转化率
(4)采取一定措施可防止钢铁腐蚀.下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液.
①在a~c装置中,能保护铁的是
bc
bc
(填字母).②若用d装置保护铁,X极的电极材料应是
锌
锌
(填名称).
化学反应与能量有比不可分的关系,回答下列问题.
Ⅰ:已知31g白磷变为31g红磷释放能量.试回答:
(1)上述变化属于
(2)31g白磷具有的能量_
(3)31g白磷完全燃烧释放的能量_
Ⅱ:A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸
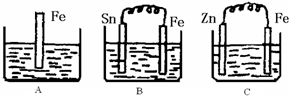
(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A
(2)一段时间后,B中Sn极附近溶液的pH
(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度=
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
Ⅲ:某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空: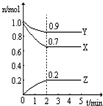
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时
查看习题详情和答案>>
Ⅰ:已知31g白磷变为31g红磷释放能量.试回答:
(1)上述变化属于
化学
化学
(填“物理”或“化学”)变化.(2)31g白磷具有的能量_
>
>
(“>”或“<”)31g红磷具有的能量,常温常压下,红磷
红磷
更稳定.(3)31g白磷完全燃烧释放的能量_
>
>
(“>”或“<”)31g红磷完全燃烧释放的能量.Ⅱ:A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸

(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
;BFe-2e-═Fe2+
Fe-2e-═Fe2+
;C2H++2e-═H2↑
2H++2e-═H2↑
.(2)一段时间后,B中Sn极附近溶液的pH
pH增大
pH增大
(填“增大”、“减小”、“不变”).(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度=
0.75
0.75
mol?L-1.此时,三个烧杯中液体质量由大到小的顺序为:C>A=B
C>A=B
(填写序号).(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
BAC
BAC
(填写序号).Ⅲ:某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:

(1)该反应的化学方程式为
3X+Y 2Z
2Z
 2Z
2Z3X+Y 2Z
2Z
. 2Z
2Z(2)反应开始至2min,以气体Z表示的平均反应速率为
0.05mol/(L.min)
0.05mol/(L.min)
.(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的
0.9
0.9
倍;②达平衡时,容器内混合气体的平均相对分子质量比起始投料时
增大
增大
(填“增大”“减小”或“相等”).