摘要:28.(1)A为碳酸钠和碳酸氢钠的混合物,(2)碳酸钠4.24 g.碳酸氢钠3.36 g,(3)1.792L.
网址:http://m.1010jiajiao.com/timu3_id_360123[举报]
混合物A由碳酸钠和碳酸氢钠组成。现有两包质量相等的混合物A:
(1)若向其中一包加入100mL 3mol/L的Ba(OH)2溶液(过量),使HCO3-、CO32-全部变为沉淀,过滤后,再向滤液中加入200mL 2mol/L的稀盐酸,溶液恰好呈中性。
①写出下列反应的离子方程式:碳酸氢钠与过量氢氧化钡的反应:_____________________________;
②混合物A中NaHCO3的质量为_____________________________g。
(2)若向另一包中先加50mL8mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50mL2mol/L的 Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下)。混合物A中Na2CO3的质量为_______________g。
查看习题详情和答案>>
(1)若向其中一包加入100mL 3mol/L的Ba(OH)2溶液(过量),使HCO3-、CO32-全部变为沉淀,过滤后,再向滤液中加入200mL 2mol/L的稀盐酸,溶液恰好呈中性。
①写出下列反应的离子方程式:碳酸氢钠与过量氢氧化钡的反应:_____________________________;
②混合物A中NaHCO3的质量为_____________________________g。
(2)若向另一包中先加50mL8mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50mL2mol/L的 Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下)。混合物A中Na2CO3的质量为_______________g。
混合物A由碳酸钠和碳酸氢钠组成.现有两包质量相等的混合物A:
(1)若向其中一包加入100 mL 3 mol/L的Ba(OH)2溶液(过量),使HCO3-、CO32-全部变为沉淀,过滤后,再向滤液中加入200 mL 2 mol/L的稀盐酸,溶液恰好呈中性.
①写出下列反应的离子方程式
碳酸氢钠与过量氢氧化钡的反应:________;
②混合物A中NaHCO3的质量为________g.
(2)若向另一包中先加50 mL 8 mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50 mL 2 mol/L的Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下).混合物A中Na2CO3的质量为________g.
碳酸钠俗称纯碱、苏打,是一种常用的日用化学品.在实验室里,可用如图所示装置,以氯化钠、二氧化碳、氨等为原料制备纯碱.实验时,先检验装置的气密性,再向各仪器中加入试剂,打开启普发生器(装置A)活塞,产生二氧化碳气体,制备纯碱.请回答以下有关问题:

(1)碳酸氢钠受热分解的化学方程式为______;实验时装置A中发生反应的化学方程式为______;C装置的锥形瓶中,装有含氨的饱和食盐水,则溶液1应为______,溶液2应为______.
(2)实验中,要注意控制二氧化碳的通入速度(以出现能数得清的连续气泡为好)和水浴的温度.实验中不能过快的通入二氧化碳的目的是______.化学实验中水浴加热法的优点为______.
实验时,锥形瓶中产生了NH4HCO3、NaCl、NaHCO3和NH4Cl的混合液.右表是四种化合物在部分温度下的溶解度.由表中数据可知,反应时水浴的温度不能超过______℃.反应结束,将反应混合液冷却到15℃左右,析出的固体应主要含有______(填化学式).
| 温度 | 10℃ | 20℃ | 30℃ | 40℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | 分解 |
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 |
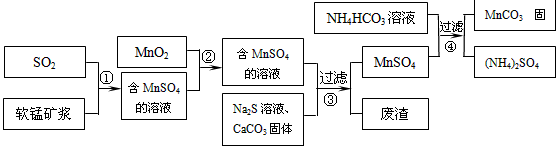
碳酸锰(MnCO3)是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业。一种制备MnCO3的生产流程如下图所示。
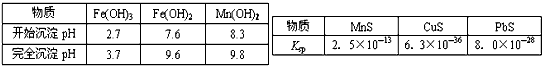
已知生成氢氧化物的pH和有关硫化物的Ksp如下表
软锰矿主要成分为MnO2,其中含有铁、铝、硅的氧化物和少量重金属化合物杂质,SO2来自工业废气。流程①中主要发生的反应有:MnO2 + SO2=MnSO4;2Fe3+ + SO2 + 2H2O=2Fe2+ + SO42- + 4H+。
(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH______(填“大”或“小”)。
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为________________________。
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀(不考虑Fe3+与S2-反应),碳酸钙的作用是__________________。
(4)反应④发生的化学反应为:MnSO4 + 2NH4HCO3=MnCO3↓+ (NH4)2SO4 + CO2↑ + H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4。加入稍过量的NH4HCO3的目的是____________,溶液的pH不能过低的原因是__________________。
(5)软锰矿中锰的浸出有两种工艺:工艺A:软锰矿浆与含SO2的工业废气反应; 工艺B:软锰矿与煤碳粉混合,焙烧后加稀硫酸溶解。其中工艺A的优点是________________________。(答对1个即可)
查看习题详情和答案>>
(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH______(填“大”或“小”)。
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为________________________。
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀(不考虑Fe3+与S2-反应),碳酸钙的作用是__________________。
(4)反应④发生的化学反应为:MnSO4 + 2NH4HCO3=MnCO3↓+ (NH4)2SO4 + CO2↑ + H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4。加入稍过量的NH4HCO3的目的是____________,溶液的pH不能过低的原因是__________________。
(5)软锰矿中锰的浸出有两种工艺:工艺A:软锰矿浆与含SO2的工业废气反应; 工艺B:软锰矿与煤碳粉混合,焙烧后加稀硫酸溶解。其中工艺A的优点是________________________。(答对1个即可)
碳酸钠俗称纯碱、苏打,是一种常用的日用化学品.在实验室里,可用如图所示装置,以氯化钠、二氧化碳、氨等为原料制备纯碱.实验时,先检验装置的气密性,再向各仪器中加入试剂,打开启普发生器(装置A)活塞,产生二氧化碳气体,制备纯碱.请回答以下有关问题:
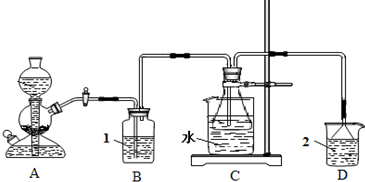
(1)碳酸氢钠受热分解的化学方程式为______;实验时装置A中发生反应的化学方程式为______;C装置的锥形瓶中,装有含氨的饱和食盐水,则溶液1应为______,溶液2应为______.
(2)实验中,要注意控制二氧化碳的通入速度(以出现能数得清的连续气泡为好)和水浴的温度.实验中不能过快的通入二氧化碳的目的是______.化学实验中水浴加热法的优点为______.
实验时,锥形瓶中产生了NH4HCO3、NaCl、NaHCO3和NH4Cl的混合液.右表是四种化合物在部分温度下的溶解度.由表中数据可知,反应时水浴的温度不能超过______℃.反应结束,将反应混合液冷却到15℃左右,析出的固体应主要含有______(填化学式).
(3)饱和食盐水,还可以通过电解过程制取烧碱.制备过程中,烧碱溶液主要在电解池的______极区产生,原因是______.
查看习题详情和答案>>

(1)碳酸氢钠受热分解的化学方程式为______;实验时装置A中发生反应的化学方程式为______;C装置的锥形瓶中,装有含氨的饱和食盐水,则溶液1应为______,溶液2应为______.
(2)实验中,要注意控制二氧化碳的通入速度(以出现能数得清的连续气泡为好)和水浴的温度.实验中不能过快的通入二氧化碳的目的是______.化学实验中水浴加热法的优点为______.
实验时,锥形瓶中产生了NH4HCO3、NaCl、NaHCO3和NH4Cl的混合液.右表是四种化合物在部分温度下的溶解度.由表中数据可知,反应时水浴的温度不能超过______℃.反应结束,将反应混合液冷却到15℃左右,析出的固体应主要含有______(填化学式).
| 温度 | 10℃ | 20℃ | 30℃ | 40℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | 分解 |
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 |