摘要:16.对于某单色光.玻璃的折射率比水的大.则此单色光在玻璃中传播时 A.其速度比在水中的大.其波长比在水中的长 B.其速度比在水中的大.其波长比在水中的短 C.其速度比在水中的小.其波长比在水中的短 D.其速度比在水中的小.其波长比在水中的长 17.图中a.b是两个位于固定斜面上的正方形物块.它们的质 量相等.F是沿水平方向作用于a上的外力.已知a.b的 接触面.a.b与斜面的接触面都是光滑的.正确的说法是 A.a.b一定沿斜面向上运动 B.a对b的作用力沿水平方向 C.a.b对斜面的正压力相等 D.a受到的合力沿水平方向的分力等于b受到的合力沿水平方向的分力 18.一简谐横波在x轴上传播.波源振动周期 T=0.1s.在某一时刻的波形如图所示.且此 时a点向下运动.则 A.波速为20m/s.波向x轴正方向传播 B.波速为10m/s.波向x轴负方向传播 C.波速为20m/s.波向x轴负方向传播 D.波速为10m/s.波向x轴正方向传播 19.如图.在正六边形的a.c两个顶点上各放一带正电的点 电荷.电量的大小都是q1.在b.d两个顶点上.各放一 带负电的点电荷.电量的大小都是q2.q1>q2.已知六边 形中心O点处的场强可用图中的四条有向线段中的一条 来表示.它是哪一条? A.E1 B.E2 C.E3 D.E4
网址:http://m.1010jiajiao.com/timu3_id_35969[举报]
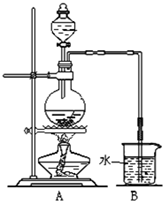 如图是某研究性学习小组利用实验室制氯气的装置设计制取氯水并进行相关实验.
如图是某研究性学习小组利用实验室制氯气的装置设计制取氯水并进行相关实验.(1)请简述如何检查该装置的气密性.
将倒气管插入盛水的烧杯中,用手捂住圆底烧瓶(或用酒精灯微热圆底烧瓶),倒气管口有气泡冒出.冷却后,倒气管中产生水柱,一段时间没有变化,说明气密性良好
将倒气管插入盛水的烧杯中,用手捂住圆底烧瓶(或用酒精灯微热圆底烧瓶),倒气管口有气泡冒出.冷却后,倒气管中产生水柱,一段时间没有变化,说明气密性良好
.(2)写出A装置中发生反应的离子方程式
MnO2+4H++2Cl-
Mn2++C12↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++C12↑+2H2O
.
| ||
(3)新制氯水能使红色布条退色.对于使红色布条退色的物质,同学们的看法不一致,认为氯水中存在的几种物质除水外都有可能.请你设计实验探究、验证,得出正确结论.
①提出假设,并进行实验探究、验证,分别简述实验的过程、现象和结论.
假设一:盐酸能使红色布条退色.探究、验证的实验过程、现象和结论为:
用玻璃棒蘸取稀盐酸滴到红色布条上,红色布条不退色,说明盐酸没有漂白作用
用玻璃棒蘸取稀盐酸滴到红色布条上,红色布条不退色,说明盐酸没有漂白作用
.假设二:
氯气使红色布条退色
氯气使红色布条退色
.探究、验证的实验过程、现象和结论为:把干燥的红色布条放入充满氯气的集气瓶中,红色布条不退色,说明氯气没有漂白作用
把干燥的红色布条放入充满氯气的集气瓶中,红色布条不退色,说明氯气没有漂白作用
.假设三:HClO能使布条退色.本假设的实验探究、验证不做要求.
②得出的结论是
次氯酸使红色布条退色
次氯酸使红色布条退色
.(4)某同学提出该装置需要进一步改进,请你写出改进的措施(或画出必要的装置图)
增加尾气吸收装置(或如图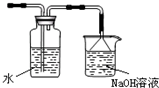 )
)
 )
)增加尾气吸收装置(或如图 )
)
. )
) 有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸.某研究性学习小组的同学们利用一小块样品,进行了以下实验.
有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸.某研究性学习小组的同学们利用一小块样品,进行了以下实验.(1)检验矿物样品中是否有Fe3+
实验用品:锤子、研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
实验步骤:
①取样:将样品用锤子敲碎,再在研钵中研细备用.
②溶解:将样品粉末倒入烧杯,加入
稀盐酸
稀盐酸
,用玻璃棒充分搅拌.③
过滤
过滤
(填操作名称).④检验:取少许溶液,
滴加KSCN溶液
滴加KSCN溶液
.实验现象:
溶液变为红色
溶液变为红色
.实验结论:矿物样品中含有Fe3+.
(2)制备氢氧化亚铁
①为了得到亚铁盐的溶液,同学们在剩余的溶液中加入过量的某种固体试剂,该试剂是(填化学式)
Fe
Fe
,反应的离子方程式是2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.②对于①中过量的固体试剂是否需要除去,同学们产生了两种观点.
甲组:认为需要过滤. 乙组:认为不需要过滤.
你支持的是组
乙
乙
(填“甲”或“乙”),理由是过量的铁粉可以防止Fe2+被氧化为Fe3+
过量的铁粉可以防止Fe2+被氧化为Fe3+
③同学们在新制得的亚铁盐溶液中加入适量新制的氢氧化钠溶液,制出的氢氧化亚铁呈
白
白
色.为使试管中的氢氧化亚铁保存的时间更长,请在右图中画出你的设计(可以加必要的文字说明).
如图1是某研究性学习小组利用实验室制氯气的装置设计制取氯水并进行相关实验.
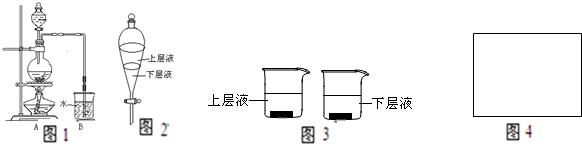
(1)A装置中发生化学反应的离子方程式为 .
(2)氯气能使湿润的红色布条褪色.对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能.请你设计实验,得出正确结论.
①提出假设假设一 .假设二 .假设三 .假设四 H2O使布条褪色
②设计实验方案
基于提出的假设,设计出实验方案(不需要作答)
③实验过程
实验①: ;实验②: .实验③:把红色布条放在水里,布条不褪色.
④得出结论 .
(3)用量筒取20mL氯水,倒入已检查完好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图2),等分层后取上层液和下层液,呈黄绿色的是 (填“上层液”或“下液”),再装入如图3所示的烧杯中,能使有色布条褪色的是 (填“上层液”或“下层液”)
(4)上述制备并吸收氯气装置的缺点是 ,如何改进 ,在图4框中画出改进的实验装置图 .
查看习题详情和答案>>

(1)A装置中发生化学反应的离子方程式为
(2)氯气能使湿润的红色布条褪色.对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能.请你设计实验,得出正确结论.
①提出假设假设一
②设计实验方案
基于提出的假设,设计出实验方案(不需要作答)
③实验过程
实验①:
④得出结论
(3)用量筒取20mL氯水,倒入已检查完好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图2),等分层后取上层液和下层液,呈黄绿色的是
(4)上述制备并吸收氯气装置的缺点是