网址:http://m.1010jiajiao.com/timu3_id_357912[举报]
【实验一】:测定硫元素的含量
I.将m1g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体.写出石英管中发生反应的化学方程式为:
| ||
| ||

Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:

问题讨论:
(1)I中,甲中所盛试剂是
(2)Ⅱ中,所加H2O2溶液需足量的理由是
发生反应的离子方程式为
(3)该黄铁矿石中硫元素的质量分数为
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
【实验二】:设计以下实验方案测定铁元素的含量

问题讨论:
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有
(6)某同学一共进行了三次滴定实验,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 26.42 | 25.05 | 24.95 |
黄铁矿是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对某黄铁矿石(主要成分为FeS2)进行如下实验探究.
【实验一】:测定硫元素的含量
I.将m1g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体.写出石英管中发生反应的化学方程式为:______.
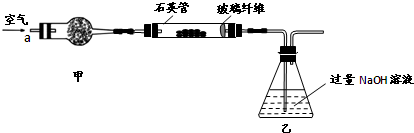
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:
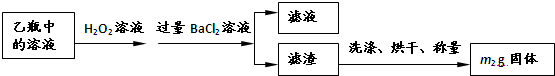
问题讨论:
(1)I中,甲中所盛试剂是______.
(2)Ⅱ中,所加H2O2溶液需足量的理由是______;
发生反应的离子方程式为______.
(3)该黄铁矿石中硫元素的质量分数为______.
【实验二】:设计以下实验方案测定铁元素的含量
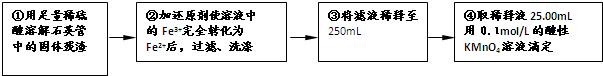
问题讨论:
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量______(填“偏大”、“偏小”或“无影响”,下同);若将稀释液久置后再用酸性KMnO4滴定,则所测得的铁元素的含量______.
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有______.
(6)某同学一共进行了三次滴定实验,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 26.42 | 25.05 | 24.95 |
如图某化学实验小组从商店买回的浓硫酸试剂标签的部分内容,该小组在课外资料中获得以下信息:浓硫酸腐蚀性很强,溶于水时释放大量的热,浓硫酸的硫酸分步电离。
|
向HSO4- ![]() SO42- + H+
SO42- + H+
由于试剂瓶口密封签已破损,他们怀疑该硫酸质量分数与标签不符,确定开展研究.
甲认为可以用一种精密仪器测量该溶液的C(H+),若C(H+) =36.8 mol•L-1,该溶液的质量分数为0.98;
乙认为,即使有精密的仪器,甲方案也不行,建议用重量分析法来测。具体设想:取一定体积该硫酸和足量BaCl2反应,过滤、洗涤、干燥沉淀,称量沉淀的质量
丙则建议用“中和滴定”进行测量,设想如下:A、准确量取一定体积的硫酸,并用适量的水稀释;B、往稀释后溶液中滴入2-3滴酚酞;C、用一定浓度的NaOH溶液滴定,直到出现滴定终点为止;D、记录消耗的NaOH溶液的体积。
回答下列问题:。
(1)乙推断“甲同学方案不可行”的理由是: 。
(2)乙方案的关键操作有两点:①确保SO42-完全反应,②洗涤沉淀,确保沉淀不夹杂质。在实验中如何认定SO42-完全反应?
。
(3)如何稀释浓硫酸溶液?
。
(4)丙方案下列操作会使测定结果偏大 。
①在滴定前未用NaOH标准溶液润洗滴定管
②滴定前滴定管尖嘴部分有气泡,滴定后滴定管尖嘴部分气泡消失
③锥形瓶用水洗干净后,未用待测液润洗
④开始时平视读数,滴定完成时俯视读数
(5)丙在实验中,分别取硫酸5.00mL,用5.00mol/L NaOH滴定三次,终点时,得到的NaOH的体积依次为35.65mL、40.62mL、35.55mL,试通过计算该硫酸是否合格.(要计算过程)
查看习题详情和答案>>(1)请写出铜跟浓硫酸反应的化学方程式:
| ||
| ||
可以证明有余酸的实验方案是
(a)再加入铁粉(b)再滴入BaCl2溶液(c)再加入银(d)再滴入Na2CO3溶液
(2)甲学生设计求余酸浓度的实验方案是测定产生气体的量.其方法有多种,请问下列方案中不可行的是
(a)将产生的气体缓缓通过预先称量盛有碱石灰的干燥管,结束反应后再次称量.
(b)将产生的气体缓缓通入酸性高锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀.
(c)用排水法测定其产生气体的体积(折算成标准状况).
(d)用排饱和NaHSO3溶液的方法测出其产生气体的体积(折算成标准状况).
(3)乙同学设计测定余酸浓度的实验方案是:测定反应后的混合液中Cu2+的量.在反应后的溶液中加蒸馏水稀释至100ml,加入足量Na2S溶液,充分反应后,过滤.洗涤.干燥、称量沉淀.请写出生成沉淀的离子方程式:
(4)根据甲、乙两同学的实验方案,除测算产生气体的物质的量或反应掉的铜的物质的量外,尚缺少的测量数据是
(5)丙同学提出甲、乙两同学的实验方案设计的复杂,为此他设计了下列较为简易的实验方案:取出反应后的铜片,进行洗涤.干燥.称量.若称得剩余铜片的质量为Wg,测得反应后溶液的体积为Vml,请计算剩余硫酸的物质的量浓度=
| 0.36-(12.8-w)/32 |
| V×1×10 -3 |
| 0.36-(12.8-w)/32 |
| V×1×10 -3 |