摘要:19.利用打点计时器验证自由落体机械能守恒时.下列器材中不必要的是 A 重物 B 纸带 C 天平 D 低压电源
网址:http://m.1010jiajiao.com/timu3_id_35773[举报]
(1)在“探究求合力的方法”的实验中,要求每次合力与分力产生相同的效果,必须: ( )
A.每次将橡皮条拉到同样的位置 B.每次把橡皮条拉直
C.每次准确读出弹簧秤的示数 D. 每次记准细绳方向
(2)某实验小组在“探究加速度与物体受力的关系”实验中,设计出如下的实验方案,其实验装置如图所示。已知小车质量![]() ,砝码盘质量
,砝码盘质量![]() ,所使用的打点计时器交流电频率
,所使用的打点计时器交流电频率![]() Hz。其实验步骤是:
Hz。其实验步骤是:
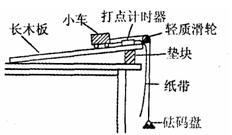
A.按图中所示安装好实验装置;
B.调节长木板的倾角,轻推小车后,
使小车能沿长木板向下做匀速运动;
C.取下细绳和砝码盘,记下砝码盘中砝码的质量![]() ;
;
D.先接通电源,再放开小车,打出一条纸带,由纸带求得小车的加速度![]() ;
;
E.重新挂上细绳和砝码盘,改变砝码盘中砝码质量,重复![]() 步骤,求得小O%M车在不同合外力
步骤,求得小O%M车在不同合外力![]() 作用下的加速度。
作用下的加速度。
回答以下问题:
①按上述方案做实验,是否要求砝码和砝码盘的总质量远小于小车的质量? (填“是”或“否”)。
②实验中打出的一条纸带如图所 示,由该纸带可求得小车的加速度![]()
![]() 。
。
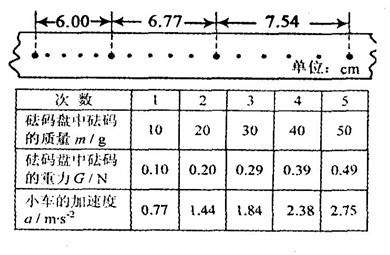
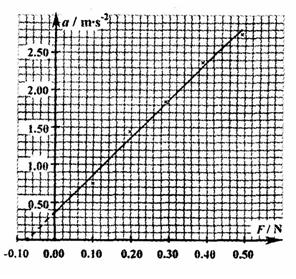
③某同学将有关数据填入他所设计的表格中,并根据表中的数据 画出![]() 图象(如图)。造成图线不过坐标原点的一条最主要原因是 ,从该图线延长线与横轴的交点可求出的物理量是 ,其大小是 。
图象(如图)。造成图线不过坐标原点的一条最主要原因是 ,从该图线延长线与横轴的交点可求出的物理量是 ,其大小是 。
同学们为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,他们准备了以下化学用品:0.20mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
(1)该实验缺少的仪器是
(2)酸液都取足量、相同体积,请你帮助完成以下面实验设计表:
(3)相同温度时,镁条与相同浓度的盐酸、醋酸反应,刚开始时两者产生气体的速率盐酸
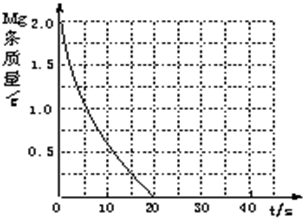
(4)若(2)中实验①镁条消失的时间是20s,则镁条剩余质量与时间关系图如右图.假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的
.请你在此图中大致画出“实验②”(用实线)、“实验④中醋酸实验”(用虚线)的镁条质量与时间关系曲线.
(5)某温度下,醋酸的电离平衡常数K(CH3COOH)=1.0×10-5.若醋酸的起始浓度为0.10mol/L,则平衡时溶液的pH值是多少?(写出计算过程)
查看习题详情和答案>>
(1)该实验缺少的仪器是
计时器
计时器
.(2)酸液都取足量、相同体积,请你帮助完成以下面实验设计表:
| 实验编号 | 温度(K) | 盐酸浓度(mol?L-1) | 醋酸浓度(mol?L-1) | 实验目的 |
| ① | 298 | 0.20 | a.实验①和②是探究 不同温度 不同温度 对镁与盐酸反应速率的影响;b.实验①和③是探究 不同浓度 不同浓度 对镁与盐酸反应速率的影响;c.实验①和④是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别. | |
| ② | 308 | 0.20 | ||
| ③ | 298 | 0.40 | ||
| ④ | 298 298 |
0.20 0.20 |
>
>
醋酸(选填“=、>或<”),镁条最先消失的是盐酸
盐酸
(选填“盐酸或醋酸”,下同);如果镁条足量,选pH相同、等体积的盐酸和醋酸与镁条反应,产生气体最多的是醋酸
醋酸
.
(4)若(2)中实验①镁条消失的时间是20s,则镁条剩余质量与时间关系图如右图.假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的
| 1 |
| 2 |
(5)某温度下,醋酸的电离平衡常数K(CH3COOH)=1.0×10-5.若醋酸的起始浓度为0.10mol/L,则平衡时溶液的pH值是多少?(写出计算过程)
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.Ⅰ(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
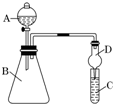
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律
(3)仪器B的名称为
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
学习了元素周期律后,同学们对第四周期过渡元素氧化物产生了浓厚的兴趣.是否只有二氧化锰能催化氯酸钾受热分解?氧化铁、氧化铜、氧化铬等对氯酸钾的受热分解有没有催化作用?对此他们进行了实验探究.请你根据要求完成下列部分实验报告.
Ⅰ课题名称:
Ⅱ实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、大试管、酒精灯、计时器等.
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ实验步骤:略
Ⅳ实验数据:
Ⅴ实验讨论:
(1)实验编号1的实验作用是
(2)实验编号3的实验中KClO3的分解率为
(3)在用Cr2O3 做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色.该刺激性气体可能是
Ⅵ实验结论:
查看习题详情和答案>>
Ⅰ课题名称:
探究二氧化锰、氧化铁、氧化铜、氧化铬的氧化能力的比较
探究二氧化锰、氧化铁、氧化铜、氧化铬的氧化能力的比较
Ⅱ实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、大试管、酒精灯、计时器等.
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ实验步骤:略
Ⅳ实验数据:
|
实验 编号 |
KClO3(g) | 氧化物 |
产生气体(mL) (已折算到标况) |
耗时(s) | ||
| 化学式 | 质量(g) | 回收 | ||||
| 1 | 0.60 | - | - | - | 10 | 480 |
| 2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.60 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
(1)实验编号1的实验作用是
对照实验
对照实验
.(2)实验编号3的实验中KClO3的分解率为
40.8
40.8
%(保留一位小数)(3)在用Cr2O3 做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色.该刺激性气体可能是
Cl2
Cl2
(填分子式),可用湿润的淀粉碘化钾
湿润的淀粉碘化钾
试纸检验.上述异常现象产生的原因是KClO3与Cr2O3发生了氧化还原反应
KClO3与Cr2O3发生了氧化还原反应
.Ⅵ实验结论:
氧化铁和二氧化锰的催化能力较好
氧化铁和二氧化锰的催化能力较好
. 某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.
某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.(1)利用Ⅰ、Ⅱ装置可制取收集气体(K2关闭,K1打开)
①下列各组物质中能直接利用这套装置进行实验的是
AC
AC
(填正确选项的标号)A.锌和稀硫酸B.双氧水和二氧化锰C.浓氨水和氧化钙D.浓盐酸和二氧化锰
②在不改变Ⅰ、Ⅱ装置及位置的前提下,若要制取收集NO气体,可采取的改进方法是装置Ⅱ内充满水;若要制取收集NO2气体,可采取的改进方法是:
将Ⅱ装置加满(难挥发的)有机溶剂
将Ⅱ装置加满(难挥发的)有机溶剂
.(2)利用Ⅰ、Ⅲ装置可验证物质的性质(K2打开,K1关闭)
①若要证明氧化性:KMnO4>Cl2>Br2,则A中加浓盐酸,B中加KMnO4,C中发生的离子反应方程式
Cl2+2Br-=2Cl-+Br2
Cl2+2Br-=2Cl-+Br2
.②若要证明乙炔为不饱和烃,则I中发生的化学反应方程式为:
CaC2+2H2O→Ca(OH)2+C2H2↑
CaC2+2H2O→Ca(OH)2+C2H2↑
.C中的现象为
溴水褪色或高锰酸钾溶液褪色
溴水褪色或高锰酸钾溶液褪色
.(3)装置Ⅲ中使用球形干燥管D可防止液体倒吸,其原因是
当气体被吸收时,液体上升到球形管中.由于球形管容积较大,导致试管中液面明显下降,使球形管口脱离液面,球形管中的液体又流回试管中,从而防止了倒吸.
当气体被吸收时,液体上升到球形管中.由于球形管容积较大,导致试管中液面明显下降,使球形管口脱离液面,球形管中的液体又流回试管中,从而防止了倒吸.
.