摘要:同时符合下列两个图象的反应(v表示反应速率.V%表示某气态生成物的体积分数.Q>0)是 (A) (B) (C) (D)
网址:http://m.1010jiajiao.com/timu3_id_356579[举报]
同时符合下列两个图象的反应(v表示反应速率,v%表示某气态生成物的体积分数)是( )
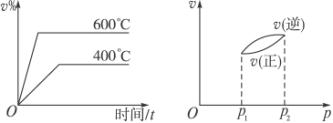
A.N2O3(g)![]() NO2(g)+NO(g);ΔH>0
NO2(g)+NO(g);ΔH>0
B.CO2(g)+C(s)![]() 2CO(g);ΔH>0
2CO(g);ΔH>0
C.3NO2(g)+H2O(l)![]() 2HNO3(l)+NO(g);ΔH<0
2HNO3(l)+NO(g);ΔH<0
D.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(l);ΔH<0
4NO(g)+6H2O(l);ΔH<0
同时符合下列两个图象的反应(v表示反应速率,v%表示某气态生成物的体积分数)是( )
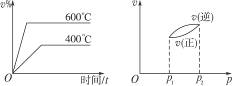
A.N2O3(g)![]() NO2(g)+NO(g);ΔH>0
NO2(g)+NO(g);ΔH>0
B.CO2(g)+C(s)![]() 2CO(g);ΔH>0
2CO(g);ΔH>0
C.3NO2(g)+H2O(l)![]() 2HNO3(l)+NO(g);ΔH<0
2HNO3(l)+NO(g);ΔH<0
D.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(l);ΔH<0
4NO(g)+6H2O(l);ΔH<0
同时符合下列两个图象的反应(v表示反应速率,v%表示某气态生成物的体积分数)是( )


A.N2O3(g) NO2(g)+NO(g);ΔH>0 NO2(g)+NO(g);ΔH>0 |
B.CO2(g)+C(s) 2CO(g);ΔH>0 2CO(g);ΔH>0 |
C.3NO2(g)+H2O(l) 2HNO3(l)+NO(g);ΔH<0 2HNO3(l)+NO(g);ΔH<0 |
D.4NH3(g)+5O2(g) 4NO(g)+6H2O(l);ΔH<0 4NO(g)+6H2O(l);ΔH<0 |
同时符合下列两个图象的反应(v是表示反应速率,V%表示某气态生成物的体积分数)的是( )
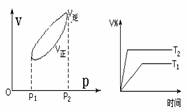
A.H2(g)+I2(g) ![]() 2HI(正反应为放热反应)
2HI(正反应为放热反应)
B.2NO2(g) ![]() N2O4(g)(正反应为放热反应)
N2O4(g)(正反应为放热反应)
C.CO2(g)+C(s) ![]() 2CO(g) (正反应为吸热反应)
2CO(g) (正反应为吸热反应)
D.4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) (正反应为放热反应)
4NO(g)+6H2O(g) (正反应为放热反应)
 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:(1)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是
B
B
(填”A”或”B”).设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2.则m1<
<
m2.(选填”<“、”=“或”>“)(2)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).该反应的平衡常数表达式K=
| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
减小
减小
(填”增大”“减小”或”不变”).在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=| 2nB |
| 3tB |
| 2nB |
| 3tB |
(3)难溶电解质在水溶液中存在着溶解平衡.在某温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数.例如:Mg(OH)2(s)?Mg2+ (aq)+2OH- (aq),某温度下Ksp=c(Mg2+)[c(OH-)]2=2×10-11.若该温度下某MgSO4溶液里c(Mg2+)=0.002mol?L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于
10
10
;该温度下,在0.20L的0.002mol?L-1MgSO4溶液中加入等体积的0.10mol?L-1的氨水溶液,该温度下电离常数K(NH3?H2O)=2×10-5,经计算有
有
(填”有”或”无”)Mg(OH)2沉淀生成.(4)常温下,向某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,则该溶液呈
碱
碱
性.在分析该溶液遇酚酞呈红色的原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中Na2CO3电离出的C| O | 2- 3 |