摘要: 电解HO和DO的“混和物 时.若电路中转移了3.75 摩尔的电子时.两极共生成 气体34.5 克.在所得气体中.H 和D 的原子个数比为 4 :1 1 :3
网址:http://m.1010jiajiao.com/timu3_id_356379[举报]
许多硫的含氧酸盐在医药、化工等方面有着重要的用途.
(1)重晶石(BaSO4)常作胃肠道造影剂.
已知:常温下,(Ksp(BaSO4)=1.1×10-10 )向BaS04悬浊液中加入硫酸,当溶液的pH=2时,溶液中 c(Ba2+)= .
(2)硫酸亚铁铵晶体[(NH4)2Fe(SO4)2?6H2O]常作分析剂.
①检验晶体中含有NH4+的方法为
②等物质的量浓度的四种稀溶液:a.(NH4)2Fe(SO4)2 b.NH4HSO4 C.(NH4)2SO4 d.(NH4)2SO3,其中c(NH4+)由大到小的顺序为 (填选项字母)o
(3)过二硫酸钾(K2S2O8)常作强氧化剂,Na2S2O3常作还原剂.
①K2S2O8溶液与酸性MnSO4溶液混合,在催化剂作用下,可以观察到溶液变为紫色,该反应的离子方程式为
②用铂作电极,电解H2SO4和K2SO4的混合溶液可以制备K2S2O8,其阳极的电极反应式为 电解过程中阴极附近溶液的pH将 (填“增大”、“减小”或“不变”)
③产品中K2S2O8的含量可用碘量法测定.操作步骤为:称取0.3g产品于碘量瓶中,加50mL水溶解;加入4.000g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以 为指示剂,用0.1000mol.L-1 Na2S2O3标准液滴定至终点(已知:I2+2S2O32-=2I-+S4O62-).重复2次,测得平均消耗标准液21.00mL.该产品 中K2S2O8的质量分数为(杂质不参加反应) (列式并计算).
查看习题详情和答案>>
(1)重晶石(BaSO4)常作胃肠道造影剂.
已知:常温下,(Ksp(BaSO4)=1.1×10-10 )向BaS04悬浊液中加入硫酸,当溶液的pH=2时,溶液中 c(Ba2+)=
(2)硫酸亚铁铵晶体[(NH4)2Fe(SO4)2?6H2O]常作分析剂.
①检验晶体中含有NH4+的方法为
②等物质的量浓度的四种稀溶液:a.(NH4)2Fe(SO4)2 b.NH4HSO4 C.(NH4)2SO4 d.(NH4)2SO3,其中c(NH4+)由大到小的顺序为
(3)过二硫酸钾(K2S2O8)常作强氧化剂,Na2S2O3常作还原剂.
①K2S2O8溶液与酸性MnSO4溶液混合,在催化剂作用下,可以观察到溶液变为紫色,该反应的离子方程式为
②用铂作电极,电解H2SO4和K2SO4的混合溶液可以制备K2S2O8,其阳极的电极反应式为
③产品中K2S2O8的含量可用碘量法测定.操作步骤为:称取0.3g产品于碘量瓶中,加50mL水溶解;加入4.000g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以
如图表示各物质之间的转化关系,A、B、C、G为单质,其中A、G为气体,F为液体.②为工业生产中常见反应,E是一种具有漂白作用的盐,Y易潮解,常用作干燥剂,M是一种两性化合物,L是一种白色胶状沉淀.
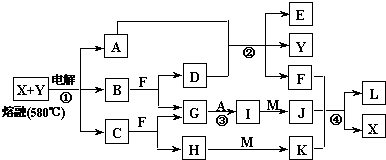
试回答下列有关问题:
(1)M的化学式
(2)X的熔点为801℃,实际工业冶炼中常常加入一定量的Y共熔,猜想工业上这样做的目的:
(3)反应②的化学方程式是
(4)反应④的离子反应方程式是
(5)用化学方程式表示E在空气中失效的反应原理
查看习题详情和答案>>

试回答下列有关问题:
(1)M的化学式
Al2O3
Al2O3
.(2)X的熔点为801℃,实际工业冶炼中常常加入一定量的Y共熔,猜想工业上这样做的目的:
降低X、Y熔化时的温度,节约能源
降低X、Y熔化时的温度,节约能源
;工业生产中,还常常利用电解X和F的混合物制取Cl2、H2和NaOH
Cl2、H2和NaOH
.(填化学式)(3)反应②的化学方程式是
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
.(4)反应④的离子反应方程式是
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.(5)用化学方程式表示E在空气中失效的反应原理
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO 2HClO
2HCl+O2↑
| ||
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO 2HClO
2HCl+O2↑
.
| ||
海水中溶解和悬浮着大量的无机物和有机物,具有巨大的开发潜力,人类除了从海水中获得食盐和水外,还获得大量的钾、镁、溴、碘等,以下说法正确的是( )
| A、用有机溶剂可萃取海水中的溴、碘 | B、海水中含有碘元素,只需将海水中的碘升华就可以得到碘单质 | C、从海水中可以得到NaCl,NaCl可以是制造化肥的原料 | D、常用电解氯化钠和氯化镁的水溶液来制得钠和镁 |