摘要: 从下列事实.不能用勒沙特列原理解释的是 A.溴水中有下列平衡Br2+H2OHBr + HBrO,当加入AgNO3溶液后.溶液颜色变浅 B.对2HI(g)H2(g)+I2(g),平衡体系增大压强可使颜色变深 C.反应CO+NO2CO2+NO+Q,升高温度可使平衡向逆反应方向移动 D.合成NH3反应.为提高NH3的产率.理论上应采取低温度的措施
网址:http://m.1010jiajiao.com/timu3_id_355226[举报]
从下列事实,不能用勒沙特列原理解释的是( )
A.溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)![]() H2(g)+I2(g),平衡体系增大压强可使颜色变深
H2(g)+I2(g),平衡体系增大压强可使颜色变深
C.反应CO+NO2![]() CO2+NO;ΔH<0,升高温度可使平衡向逆反应方向移动
CO2+NO;ΔH<0,升高温度可使平衡向逆反应方向移动
D.合成NH3反应,为提高NH3的产率,理论上应采取降低温度的措施
查看习题详情和答案>>从下列事实,找出不能用勒沙特列原理解释的是
A.在溴水中存在如下平衡: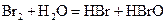 ,当加入NaOH溶液后颜色变浅 ,当加入NaOH溶液后颜色变浅 |
B.对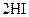  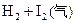 平衡体系增加压强使颜色变深 平衡体系增加压强使颜色变深 |
C.反应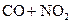  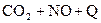 升高温度使平衡向逆方向移动 升高温度使平衡向逆方向移动 |
D.合成氨反应: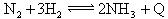 ,为使氨的产率提高,理论上应采取低温高压的措施 ,为使氨的产率提高,理论上应采取低温高压的措施 |
(08龙岩一中二模)从下列事实,找出不能用勒沙特列原理解释的是()
A.在溴水中存在如下平衡:Br2+H2O![]() HBr +HBrO,当加入NaOH溶液后颜色变浅
HBr +HBrO,当加入NaOH溶液后颜色变浅
B.对![]()
![]()
![]() 平衡体系增加压强使颜色变深
平衡体系增加压强使颜色变深
C.反应CO+NO2![]() CO2+NO △H<0 升高温度使平衡向逆方向移动
CO2+NO △H<0 升高温度使平衡向逆方向移动
D.合成氨反应:N2+3H2![]() 2NH3 △H<0,为使氨的产率提高,理论上应采取低温高压的措施
2NH3 △H<0,为使氨的产率提高,理论上应采取低温高压的措施
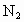 和
和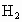 ,并将生成的
,并将生成的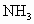 及时地从混合气体中分离出去,这样做有利于合成氨的反应
及时地从混合气体中分离出去,这样做有利于合成氨的反应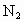 和
和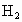 ,并将生成的
,并将生成的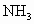 及时地从混合气体中分离出去,这样做有利于合成氨的反应
及时地从混合气体中分离出去,这样做有利于合成氨的反应