摘要:4. 工业生产中的废渣.废水.废气和生活污水的任意排放.农业生产中施用化肥.农 药随雨水流入江.河.湖水中都造成水的污染.受污染的水危及人和动物的生命.危害 工农业生产,降低产品质量和产量.且使地球上能利用的淡水资源更加缺乏.因此需采 取各种科学方法预防和消除对水源的污染.保护和改善水质.人人增强环境保护意识. 人人珍惜每一滴水.
网址:http://m.1010jiajiao.com/timu3_id_355143[举报]
工业上由FeS2制H2SO4的转化关系如下:

填写下列空白:
(1)吸收塔中发生反应的化学方程式为
(2)接触室内发生的反应为:SO2(g)+
O2(g)
SO3(g)△H=a kJ?mol-1 下表为不同温度(T)下该反应的化学平衡常数(K):
①根据上表数据及化学平衡理论,上述反应中a
②K值越大,表明反应达到平衡时
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是
A.Fe2O3
Fe
FeSO4
B.Fe2O3
Fe2(SO4)3
FeSO
C.Fe2O3
Fe
FeSO4
D.Fe2O3
Fe
FeSO4
(4)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏(CaSO4?2H2O).求:22.4m3(标准状况下)的尾气可制得石膏多少千克?(设二氧化硫的利用率为80.0%)
查看习题详情和答案>>

填写下列空白:
(1)吸收塔中发生反应的化学方程式为
SO3+H2O=H2SO4
SO3+H2O=H2SO4
.(2)接触室内发生的反应为:SO2(g)+
| 1 |
| 2 |
| 催化剂 |
| △ |
| T/K | 673 | 723 | 823 | 923 |
| K | 423 | 37.4 | 20.5 | 4.68 |
<
<
0(填“>”或“<”).②K值越大,表明反应达到平衡时
C
C
(填标号).A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是
B
B
(填标号)A.Fe2O3
| CO |
| 高温 |
| 稀硫酸 |
B.Fe2O3
| 稀硫酸 |
| 铁屑 |
C.Fe2O3
| 铁粉 |
| 高温 |
| 稀硫酸 |
D.Fe2O3
| H2 |
| 高温 |
| 硫酸铜溶液 |
(4)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏(CaSO4?2H2O).求:22.4m3(标准状况下)的尾气可制得石膏多少千克?(设二氧化硫的利用率为80.0%)
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收。请回答下列问题:
(1)煅烧黄铁矿形成的炉气必须经除尘、洗涤、干燥后进入 (填设备名称),其主要目的是 。
(2)催化氧化所使用的催化剂钒触媒(V2O5)能加快二氧化硫氧化速率,此过程中产生了一连串的中间体(如图1)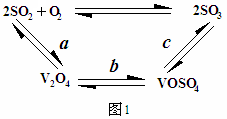
其中a、c二步反应的化学方程式可表示为: 、 。
(3)550℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(P)的关系如图2所示,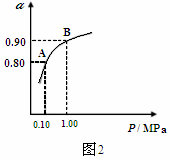
则:将2.0mol SO2和1.0mol O2置于5L密闭容器中,反应达平衡后,体系总压强为0.10M Pa,A与B表示不同压强下的SO2转化率,通常情况下工业生产中采用常压的原因是: 。
(4)为循环利用催化剂,科研人员最新研制了一种离子交换法回收钒的新工艺,回收率达91.7%以上。已知废钒催化剂中含有V2O5、VOSO4及不溶性残渣,查阅资料知:VOSO4可溶于水,V2O5难溶于水,NH4VO3难溶于水。该工艺的流程如图如下: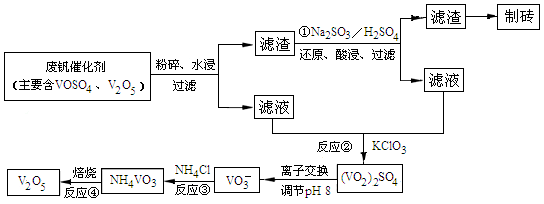
则反应①②③④中属于氧化还原反应的是 (填数字序号),反应①的离子方程式为 ,该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图试建议控制氯化铵系数和温度: 、 。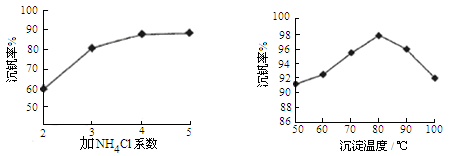
工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾.为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品.请按要求回答下列问题:
(1)工业制备硫酸时硫铁矿燃烧的设备是______,反应的化学方程式为______.
(2)将尾气通入氨水中,能发生多个反应,写出其中可能发生的任意一个氧化还原反应的化学方程式:______.
(3)能用于测定硫酸尾气中SO2含量的是______.(填字母)
A.NaOH溶液、酚酞试液
B.KMn04溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞试液
(4)在制各硫酸的过程中,对废液、废热和废渣的处理正确的是:.
a.污水用石灰乳处理
b.废渣用来造水泥、炼铁
c.设置“废热”锅炉产生蒸气来供热或发电.
查看习题详情和答案>>
工业上由FeS2制H2SO4的转化关系如下:

填写下列空白:
(1)吸收塔中发生反应的化学方程式为______.
(2)接触室内发生的反应为:SO2(g)+ O2(g)
O2(g) SO3(g)△H=a kJ?mol-1 下表为不同温度(T)下该反应的化学平衡常数(K):
SO3(g)△H=a kJ?mol-1 下表为不同温度(T)下该反应的化学平衡常数(K):
| T/K | 673 | 723 | 823 | 923 |
| K | 423 | 37.4 | 20.5 | 4.68 |
②K值越大,表明反应达到平衡时______(填标号).
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是______(填标号)
A.Fe2O3
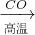 Fe
Fe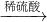 FeSO4
FeSO4B.Fe2O3
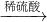 Fe2(SO4)3
Fe2(SO4)3 FeSO
FeSO C.Fe2O3
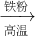 Fe
Fe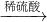 FeSO4
FeSO4D.Fe2O3
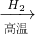 Fe
Fe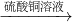 FeSO4
FeSO4(4)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏(CaSO4?2H2O).求:22.4m3(标准状况下)的尾气可制得石膏多少千克?(设二氧化硫的利用率为80.0%) 查看习题详情和答案>>
工业上由FeS2制H2SO4的转化关系如下:
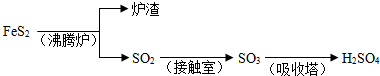
填写下列空白:
(1)已知吸收塔中每40gSO3气体被水完全吸收生成液态硫酸放出65.15kJ,写出该反应的热化学方程式______;
(2)接触室内发生的反应为:
SO2(g)+
O2(g)
SO3(g)△H=a kJ?mol-1
下表为不同温度(T)下该反应的化学平衡常数(K):
①根据上表数据及化学平衡理论,上述反应中a______0(填“>”或“<”);
②K值越大,表明反应达到平衡时______(填标号).
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是______(填标号);
A.Fe2O3
Fe
FeSO4;B.Fe2O3
Fe2(SO4)3
FeSO4;C.Fe2O3
Fe
FeSO4
(4)为了探究接触室里催化剂颗粒(粗颗粒和细颗粒),反应的温度(673K和723K),反应的压强(101Kpa和1010Kpa)对反应速率的影响,通过变换这些实验条件,至少需要完成______个实验然后进行对比得出结论;
(5)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏(CaSO4?2H2O).求:22.4m3(标准状况下)的尾气可制得石膏______千克;(取两位有效数字)(设二氧化硫的利用率为80.0% )
(6)科学家研究出以图所示装置用电化学原理生产硫酸的新工艺,其阳极的电极反应式为______,总反应的化学方程式为______.
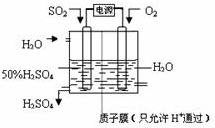
查看习题详情和答案>>

填写下列空白:
(1)已知吸收塔中每40gSO3气体被水完全吸收生成液态硫酸放出65.15kJ,写出该反应的热化学方程式______;
(2)接触室内发生的反应为:
SO2(g)+
| 1 |
| 2 |
| ||
| △ |
下表为不同温度(T)下该反应的化学平衡常数(K):
| T/K | 673 | 723 | 823 | 923 |
| K | 423 | 37.4 | 20.5 | 4.68 |
②K值越大,表明反应达到平衡时______(填标号).
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是______(填标号);
A.Fe2O3
| ||
| 高温 |
| 浓硫酸 |
| 浓硫酸 |
| 铁屑 |
| 铁粉 |
| 高温 |
| 浓硫酸 |
(4)为了探究接触室里催化剂颗粒(粗颗粒和细颗粒),反应的温度(673K和723K),反应的压强(101Kpa和1010Kpa)对反应速率的影响,通过变换这些实验条件,至少需要完成______个实验然后进行对比得出结论;
(5)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏(CaSO4?2H2O).求:22.4m3(标准状况下)的尾气可制得石膏______千克;(取两位有效数字)(设二氧化硫的利用率为80.0% )
(6)科学家研究出以图所示装置用电化学原理生产硫酸的新工艺,其阳极的电极反应式为______,总反应的化学方程式为______.
