网址:http://m.1010jiajiao.com/timu3_id_354267[举报]
氯化亚铁溶液中滴加硫氰化钾溶液,再滴加双氧水,立即出现血红色,后红色又褪去呈黄色并伴有气泡产生,针对该实验现象,某实验小组的同学进行了探究
一、现象分析
假设A:气泡是H2O2分解产生的O2
假设B:气泡是KSCN被氧化为N2、SO2、CO2等
假设C:红色褪去的原因是KSCN被氧化成了其它物质
二、实验探究
探究1
|
实验操作 |
实验现象 |
结论 |
|
①1mL 0.1mol/L的FeCl2溶液中加2滴KSCN溶液 |
溶液不变红 |
Fe2+遇SCN-不变红 |
|
②向①的溶液中加3%的H2O21滴并振荡 |
立即出现血红色 振荡后不褪色 |
加入H2O2后溶液中 出现了 (离子符号) |
|
③向②的溶液中继续加H2O2溶液 |
溶液中出现大量气泡 血红色褪去 |
|
|
④用带火星的木条检验③中的气体 |
木条复燃 |
则假设 成立 |
探究2
|
实验操作 |
实验现象 |
结论 |
|
①取2ml KSCN溶液向其中加入几滴BaCl2溶液和稀盐酸 |
无明显现象 |
|
|
②向①所得的溶液中滴加3%的H2O2 |
溶液中出现白色沉淀并有少量气泡
|
白色沉淀为BaSO4
|
|
③将6%的H2O2溶液加入KSCN固体中,生成的气体依次通过品红溶液,酸性KMnO4溶液和澄清的石灰水 |
|
KSCN被H2O2氧化生成了SO2和CO2气体 |
三、问题与讨论
(1)探究1中,H2O2分解速度很快的原因
(2)探究1中,说明还原性Fe2+ SCN-
(3)探究2中,酸性KMnO4溶液的作用是
能证明生成了CO2的现象是
(4)若SCN -被H2O2氧化得到N2、SO2、CO2和SO42-,且SO2与SO42-的物质的量比为1:1,试写出该反应的离子方程式
查看习题详情和答案>>
氯化亚铁溶液中滴加硫氰化钾溶液,再滴加双氧水,立即出现血红色,后红色又褪去呈黄色并伴有气泡产生,针对该实验现象,某实验小组的同学进行了探究
一、现象分析
假设A:气泡是H2O2分解产生的O2
假设B:气泡是KSCN被氧化为N2、SO2、CO2等
假设C:红色褪去的原因是KSCN被氧化成了其它物质
二、实验探究
探究1
| 实验操作 | 实验现象 | 结论 |
| ①1mL 0.1mol/L的FeCl2溶液中加2滴KSCN溶液 | 溶液不变红 | Fe2+遇SCN-不变红 |
| ②向①的溶液中加3%的H2O21滴并振荡 | 立即出现血红色 振荡后不褪色 | 加入H2O2后溶液中 出现了 (离子符号) |
| ③向②的溶液中继续加H2O2溶液 | 溶液中出现大量气泡 血红色褪去 | |
| ④用带火星的木条检验③中的气体 | 木条复燃 | 则假设 成立 |
探究2
| 实验操作 | 实验现象 | 结论 |
| ①取2ml KSCN溶液向其中加入几滴BaCl2溶液和稀盐酸 | 无明显现象 | |
| ②向①所得的溶液中滴加3%的H2O2 | 溶液中出现白色沉淀并有少量气泡 | 白色沉淀为BaSO4 |
| ③将6%的H2O2溶液加入KSCN固体中,生成的气体依次通过品红溶液,酸性KMnO4溶液和澄清的石灰水 | | KSCN被H2O2氧化生成了SO2和CO2气体 |
(1)探究1中,H2O2分解速度很快的原因
(2)探究1中,说明还原性Fe2+ SCN-
(3)探究2中,酸性KMnO4溶液的作用是
能证明生成了CO2的现象是
(4)若SCN -被H2O2氧化得到N2、SO2、CO2和SO42-,且SO2与SO42-的物质的量比为1:1,试写出该反应的离子方程式 查看习题详情和答案>>
离子方程式正误判断专题(正确的选A,错误的选B)
过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O
苯酚钠溶液中通入少量:![]() -O-+CO2+H2O→
-O-+CO2+H2O→![]() -OH+HCO3-
-OH+HCO3-
FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
浓氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO32-+H2O
硫酸铜溶液中通入硫化氢 Cu2++H2S=CuS↓+2H+
氯化铝溶液中加入过量氨水 Al3++4NH3·H2O=AlO2-+4NH4++2H2O
碳酸氢钠溶液中加入过量氢氧化钠溶液HCO3-+OH-=CO32-+H2O
向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液
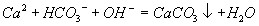
金属铝溶于氢氧化钠溶液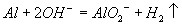
用氢氧化钠溶液吸收二氧化碳
Fe2(SO4)3的酸性溶液中通入足量硫化氢![]()
次氯酸钙溶液中通入过量二氧化碳Ca2++2ClO-+H2O+CO2 == CaCO3↓+2HClO
碳酸氢镁溶液中加入足量的烧碱溶液:Mg2++2HCO3-+2OH-=MgCO3↓+CO32-+2H2O
用氨水吸收少量二氧化硫:NH3·H2O+SO2 == NH![]() +HSO
+HSO![]()
硝酸铁溶液中加过量氨水:Fe3++3 NH3·H2O == Fe(OH)3↓+3NH![]()
硫化钠溶于水中 S2-+2H2O H2S↑+2OH-
实验室制取氯气 MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
铜与稀硝酸反应 3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O
Ca(OH)2溶液中加入等物质的量的NaHCO3
Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
NaHCO3的水解:HCO3-+H2O H3O+ +CO32-
H3O+ +CO32-
金属铝溶于NaOH溶液:Al+2OH-=AlO2-+H2↑
钢铁吸氧腐蚀的正极反应式:4OH--4e-=O2+2H2O
硫酸亚铁溶液与过氧化氢溶液混合:Fe2++2H2O2+4H+=Fe3++4H2O
小苏打溶液与稀硫酸混合CO32-+2H+=CO2↑+H2O
大理石溶解于醋酸CaCO3+2H+=Ca2++CO2↑+H2O
三氯化铝溶液加热蒸干 Al3++3H2O=Al(OH)3↓+3H+
硫酸铝溶液中加入过量氨水 Al3++3OH—══Al(OH)3↓
电解饱和食盐水 2Cl—+2H2O H2↑+C12↑+20H—
H2↑+C12↑+20H—
碳酸钙与盐酸反应 CaCO3+2H+═Ca2++CO2↑ +H2O
查看习题详情和答案>>一、现象分析
假设A:气泡是H2O2分解产生的O2
假设B:气泡是KSCN被氧化为N2、SO2、CO2等
假设C:红色褪去的原因是KSCN被氧化成了其它物质
二、实验探究
探究1
| 实验操作 | 实验现象 | 结论 |
| ①1mL 0.1mol/L的FeCl2溶液中加2滴KSCN溶液 | 溶液不变红 | Fe2+遇SCN-不变红 |
| ②向①的溶液中加3%的H2O21滴并振荡 | 立即出现血红色 振荡后不褪色 | 加入H2O2后溶液中 出现了 (离子符号) |
| ③向②的溶液中继续加H2O2溶液 | 溶液中出现大量气泡 血红色褪去 | |
| ④用带火星的木条检验③中的气体 | 木条复燃 | 则假设 成立 |
探究2
| 实验操作 | 实验现象 | 结论 |
| ①取2ml KSCN溶液向其中加入几滴BaCl2溶液和稀盐酸 | 无明显现象 | |
| ②向①所得的溶液中滴加3%的H2O2 | 溶液中出现白色沉淀并有少量气泡 | 白色沉淀为BaSO4 |
| ③将6%的H2O2溶液加入KSCN固体中,生成的气体依次通过品红溶液,酸性KMnO4溶液和澄清的石灰水 | | KSCN被H2O2氧化生成了SO2和CO2气体 |
(1)探究1中,H2O2分解速度很快的原因
(2)探究1中,说明还原性Fe2+ SCN-
(3)探究2中,酸性KMnO4溶液的作用是
能证明生成了CO2的现象是
(4)若SCN -被H2O2氧化得到N2、SO2、CO2和SO42-,且SO2与SO42-的物质的量比为1:1,试写出该反应的离子方程式