摘要:硫与铜的反应
网址:http://m.1010jiajiao.com/timu3_id_354133[举报]
铜的冶炼大致可分为:
(1)富集,将硫化物矿进行浮选;
(2)焙烧,主要反应为:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣);
(3)制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2↑;
(4)电解精炼.
下列说法正确的是( )
(1)富集,将硫化物矿进行浮选;
(2)焙烧,主要反应为:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣);
(3)制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2↑;
(4)电解精炼.
下列说法正确的是( )
查看习题详情和答案>>
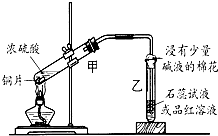 浓硫酸与铜的反应用了如图所示的装置,请回答下列问题.
浓硫酸与铜的反应用了如图所示的装置,请回答下列问题.(1)若试管乙中装的是石蕊试液,则反应过程中观察到乙中的现象是
石蕊试液变红
石蕊试液变红
;若试管乙中装的是品红溶液,则反应过程中观察到乙中的现象是品红溶液褪色
品红溶液褪色
.(2)反应结束后在试管甲的底部常可见到一些白色固体,该固体可能是
CuSO4
CuSO4
(填化学式).待试管甲内液体冷却后,将试管中的液体慢慢倒入另一支盛有少量水的试管中,观察溶液的颜色.这一步操作的目的是要证实溶液中有Cu2+ 存在
溶液中有Cu2+ 存在
.(3)写出上述试管甲中发生反应的化学方程式
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
,若收集到标准状况下气体0.56L,则反应中转移电子的物质的量为
| ||
0.05 mol
0.05 mol
.铜的冶炼大致可分为:①富集,将硫化物矿进行浮选;②焙烧,主要反应为:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣);③制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2↑;④电解精炼铜.下列说法正确的是( )
| A、上述灼烧过程的尾气均可直接排空 | B、上述过程中,由6molCuFeS2制取6molCu时共消耗12molO2 | C、在反应2Cu2O+Cu2S=6Cu+SO2↑中,只有Cu2O作氧化剂 | D、电解精炼铜时,粗铜应与外接电源的正极相连接 |