摘要:25mol电子时 (1)电解后所得溶液中溶质的质量为多少克? (2)在标准状况下.阳极上放出气体多少升?
网址:http://m.1010jiajiao.com/timu3_id_353944[举报]
如下图所示,用铅蓄电池电解100g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5g。下列说法正确的是
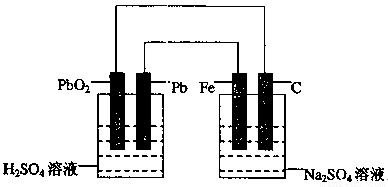
A.电路中转移0.25mol电子
B.铅蓄电池中消耗0.5mol H2SO4
C.铅蓄电池的负极反应式为:PbSO4+2H2O—2e-=PbO2+4H++SO2-4
D.Fe电极发生的电极反应为Fe—2e-=Fe2+
查看习题详情和答案>>
如下图所示,用铅蓄电池电解100g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5g。下列说法正确的是
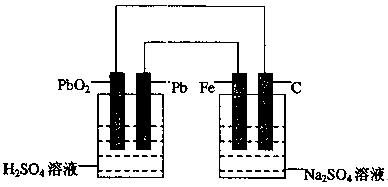
A.电路中转移0.25mol电子
B.铅蓄电池中消耗0.5mol H2SO4
C.铅蓄电池的负极反应式为:PbSO4+2H2O—2e-=PbO2+4H++SO2-4
D.Fe电极发生的电极反应为Fe—2e-=Fe2+
查看习题详情和答案>>如下图所示,用铅蓄电池电解100g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5g。下列说法正确的是
A.电路中转移0.25mol电子
B.铅蓄电池中消耗0.5molH2SO4
C.铅蓄电池的负极反应式为:PbSO4+2H2O—2e-=PbO2+4H++SO2-4
D.Fe电极发生的电极反应为Fe—2e-=Fe2+
查看习题详情和答案>>
如下图所示,用铅蓄电池电解100g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5g。下列说法正确的是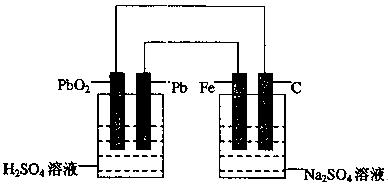
| A.电路中转移0.25mol电子 |
| B.铅蓄电池中消耗0.5mol H2SO4 |
| C.铅蓄电池的负极反应式为:PbSO4+2H2O—2e-=PbO2+4H++SO2-4 |
| D.Fe电极发生的电极反应为Fe—2e-=Fe2+ |
 熔融盐燃料电池具有高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO32--52e-═34CO2+10H2O.试回答下列问题:
熔融盐燃料电池具有高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO32--52e-═34CO2+10H2O.试回答下列问题:(1)该燃料电池的化学反应方程式为
2C4H10+13O2=8CO2+10H2O
2C4H10+13O2=8CO2+10H2O
.(2)正极电极反应式为
O2+2CO2+4e-=2CO32-或13O2+26CO2+52e-=26CO32-
O2+2CO2+4e-=2CO32-或13O2+26CO2+52e-=26CO32-
.(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定.为此,必须在通入的空气中加入一种物质,加入的物质是
CO2
CO2
.(4)某学生想用该燃料电池和如图所示装置来电解饱和食盐水.
①写出该反应的离子方程式
2Cl-+2H2O
Cl2↑+H2↑+2OH-
| ||
2Cl-+2H2O
Cl2↑+H2↑+2OH-
.
| ||
②若电解后得到200mL3.25mol/LNaOH溶液,则消耗C4H10 的体积在标准状况下为
560
560
mL.