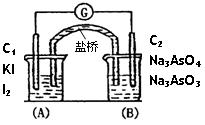
摘要:20.已知反应AsO43-+2I-+2H+AsO33- +I2+H2O是可逆反应.现设计如图2-33所示的实验装置.A烧杯中装有Na3AsO4和Na3AsO3溶液.B烧杯中装有I2和KI溶液.两烧杯用一倒置的装有饱和氯化钾的U形管相连.此装置称为盐桥.其作用是避免两烧杯中的电解质溶液相混合.又使两烧杯中的电解质溶液能导电.C1.C2为惰性电极.现进行如下操作:a.向B溶液中滴入浓盐酸.发现电流计指针发生偏转.b.若改向B溶液中滴入40%的氢氧化钠溶液.发现电流计指针向相反方向偏转.试回答下列问题: (1)电流计指针为什么能发生偏转 . (2)两次操作中,电流计指针的偏转方向为什么相反?用化学平衡原理解释. (3)写出a操作中C1棒上和 b操作中C2棒上发生的电极反应方程式. a操作中C1棒 b操作中C2棒
网址:http://m.1010jiajiao.com/timu3_id_351469[举报]
已知反应AsO43- +2I- +2H+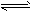 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作:
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作:
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液结果发现电流计指针均发生偏转。
据此,下列判断正确的是
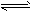 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作:
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作: Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液结果发现电流计指针均发生偏转。
据此,下列判断正确的是
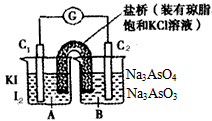
[ ]
A.操作I过程中,C1为正极
B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液
C.操作I过程中,C2棒上发生的反应为:AsO43-+2H+ +2e-=AsO33-+H2O
D.操作Ⅱ过程中,C1棒上发生的反应为:2I- =I2 +2e-
查看习题详情和答案>>
B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液
C.操作I过程中,C2棒上发生的反应为:AsO43-+2H+ +2e-=AsO33-+H2O
D.操作Ⅱ过程中,C1棒上发生的反应为:2I- =I2 +2e-
已知反应AsO43- +2I- +2H+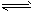 AsO33-+ I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:
AsO33-+ I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40%NaOH溶液结果发现电流计指针均发生偏转据此,下列判断正确的是
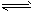 AsO33-+ I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:
AsO33-+ I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40%NaOH溶液结果发现电流计指针均发生偏转据此,下列判断正确的是

[ ]
A. 操作Ⅰ过程中,C1为正极
B. 操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液
C. Ⅰ操作过程中,C2棒上发生的反应为AsO43-+2H++2e-→AsO33-+H2O
D. Ⅱ操作过程中,C1棒上发生的反应为2I-→I2+2e-
查看习题详情和答案>>
B. 操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液
C. Ⅰ操作过程中,C2棒上发生的反应为AsO43-+2H++2e-→AsO33-+H2O
D. Ⅱ操作过程中,C1棒上发生的反应为2I-→I2+2e-
已知反应AsO43—+2I—+2H+ ![]() AsO33—+I2+H2O是可逆反应。设计如图装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导体作用),分别进行下述操作:(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,(Ⅱ)向(B)烧杯中逐滴加入40%NaOH溶液。结果均发现电流计指针偏转。据此,下列判断正确的是
AsO33—+I2+H2O是可逆反应。设计如图装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导体作用),分别进行下述操作:(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,(Ⅱ)向(B)烧杯中逐滴加入40%NaOH溶液。结果均发现电流计指针偏转。据此,下列判断正确的是

A.两次操作过程中指针偏转方向相同
B.两次操作过程中指针偏转方向相反
C.(Ⅰ)操作过程中C2棒上发生的反应为:AsO43—+2e—+2H+= AsO33—+H2O
D.(Ⅱ)操作过程中C1棒上发生的反应为:2I——2e— = I2
查看习题详情和答案>>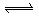 AsO33—+I2+H2O是可逆反应。设计如图装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导体作用),分别进行下述操作:(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,(Ⅱ)向(B)烧杯中逐滴加入40%NaOH溶液。结果均发现电流计指针偏转。据此,下列判断正确的是
AsO33—+I2+H2O是可逆反应。设计如图装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导体作用),分别进行下述操作:(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,(Ⅱ)向(B)烧杯中逐滴加入40%NaOH溶液。结果均发现电流计指针偏转。据此,下列判断正确的是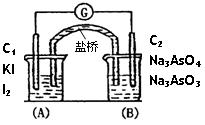
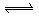 AsO33—+I2+H2O是可逆反应。设计如图装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导体作用),分别进行下述操作:(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,(Ⅱ)向(B)烧杯中逐滴加入40%NaOH溶液。结果均发现电流计指针偏转。据此,下列判断正确的是
AsO33—+I2+H2O是可逆反应。设计如图装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导体作用),分别进行下述操作:(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,(Ⅱ)向(B)烧杯中逐滴加入40%NaOH溶液。结果均发现电流计指针偏转。据此,下列判断正确的是