摘要:20.铅从单质到化合物都有着广泛的应用.如制造焊锡.铅蓄电池.化工耐酸设备以及X射线的防护材料等.铅的氧化物主要有三种:PbO.PbO2和Pb3O4.请回答下列问题: ①铅位于元素周期表中第 周期第 族, ②PbO2是一种两性氧化物.试写出PbO2和NaOH浓溶液反应的离子方程式: , ③铅蓄电池是目前使用最普及的一种蓄电池.它是以Pb.PbO2为电极.以H2SO4溶液为电解液.由于硫酸浓度较大.实际参加反应的是HSO4-.而不是SO42-.铅蓄电池放电时负极反应和电池总反应分别为: 负极反应式 Pb+ HSO4--2e-=PbSO4+H+ 电池总反应式 Pb+PbO2+2 H2SO4=2 PbSO4+2H2O 则铅蓄电池放电时正极反应式为: . (2)在真空密闭容器中加入一定量的PH4I固体.在一定温度下发生反应: PH4I(s) PH3.4PH3(g) P4(g) +6H2(g). 2HI(g) H2(g) +I2(g) 平衡后.增大压强.容器内n (PH4I) (填“增加 .“减少 或“不变 .下同).n (I2) .
网址:http://m.1010jiajiao.com/timu3_id_351365[举报]
铅从单质到化合物都有着广泛的应用,如制造焊锡、铅蓄电池、化工耐酸设备以及X射线的防护材料等。铅的氧化物主要有三种:PbO、PbO2和Pb3O4。请回答下列问题:
(1)①铅位于元素周期表中第_________周期第_________族;
②PbO2是一种两性氧化物,试写出PbO2和NaOH浓溶液反应的离子方程式:________________________________;
③铅蓄电池是目前最普及的一种蓄电池。它是以Pb、PbO2为电极,以H2SO4溶液为电解液。由于硫酸浓度较大,实际参加反应的是![]() ,而不是
,而不是![]() 。铅蓄电池放电时负极反应和电池总反应分别为:
。铅蓄电池放电时负极反应和电池总反应分别为:
反极反应式
Pb+![]() -2e-====PbSO4+H+
-2e-====PbSO4+H+
电池总反应式
Pb+PbO2+2H2SO4====2PbSO4+2H2O
则铅蓄电池放电时正极反应式为:____________________________________________。
(2)在真空密闭容器中加入一定量的PH4I固体,在一定温度下发生反应:
PH4I(s)![]() PH3(g)+HI(g),4PH3(g)
PH3(g)+HI(g),4PH3(g) ![]() P4(g)+6H2(g),2HI(g)
P4(g)+6H2(g),2HI(g) ![]() H2(g)+I2(g)平衡后,增大压强,溶器内n(PH4I)____________(填“增加”“减少”或“不变”,下同),n(I2) ____________。
H2(g)+I2(g)平衡后,增大压强,溶器内n(PH4I)____________(填“增加”“减少”或“不变”,下同),n(I2) ____________。
 下表是元素周期表的一部分,表中所列字母分别代表十种化学元素,就表中字母所代表的元素回答下列问题.
下表是元素周期表的一部分,表中所列字母分别代表十种化学元素,就表中字母所代表的元素回答下列问题.(1)铅(原子序数为82)从单质到其化合物都有着广泛的应用,如制造焊锡、铅蓄电池、化工耐酸设备以及X射线的防护材料等.铅的氧化物主要有三种:PbO、PbO2和Pb3O4.请回答下列问题:
①铅位于元素周期表中第
六
六
周期第ⅣA
ⅣA
族;②PbO2是一种两性氧化物,试写出PbO2和NaOH浓溶液反应的离子方程式:
PbO2+2NaOH═Na2PbO3+H2O
PbO2+2NaOH═Na2PbO3+H2O
.(2)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图


(3)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑.请预测首先被用来与F2反应制备稀有气体化合物的元素是
j
j
(填写字母).利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式XeO3+3NaBrO3
3NaBrO4+Xe
| ||
XeO3+3NaBrO3
3NaBrO4+Xe
.
| ||
下表是元素周期表的一部分,表中所列字母分别代表十种化学元素,就表中字母所代表的元素回答下列问题.
(1)铅(原子序数为82)从单质到其化合物都有着广泛的应用,如制造焊锡、铅蓄电池、化工耐酸设备以及X射线的防护材料等.铅的氧化物主要有三种:PbO、PbO2和Pb3O4.请回答下列问题:
①铅位于元素周期表中第______周期第______族;
②PbO2是一种两性氧化物,试写出PbO2和NaOH浓溶液反应的离子方程式:______.
(2)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图______.
(3)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑.请预测首先被用来与F2反应制备稀有气体化合物的元素是______(填写字母).利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式______.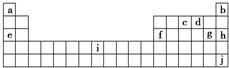
查看习题详情和答案>>
(1)铅(原子序数为82)从单质到其化合物都有着广泛的应用,如制造焊锡、铅蓄电池、化工耐酸设备以及X射线的防护材料等.铅的氧化物主要有三种:PbO、PbO2和Pb3O4.请回答下列问题:
①铅位于元素周期表中第______周期第______族;
②PbO2是一种两性氧化物,试写出PbO2和NaOH浓溶液反应的离子方程式:______.
(2)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图______.
(3)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑.请预测首先被用来与F2反应制备稀有气体化合物的元素是______(填写字母).利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式______.

下表是元素周期表的一部分,表中所列字母分别代表十种化学元素,就表中字母所代表的元素回答下列问题.
(1)铅(原子序数为82)从单质到其化合物都有着广泛的应用,如制造焊锡、铅蓄电池、化工耐酸设备以及X射线的防护材料等.铅的氧化物主要有三种:PbO、PbO2和Pb3O4.请回答下列问题:
①铅位于元素周期表中第______周期第______族;
②PbO2是一种两性氧化物,试写出PbO2和NaOH浓溶液反应的离子方程式:______.
(2)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图______.
(3)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑.请预测首先被用来与F2反应制备稀有气体化合物的元素是______(填写字母).利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式______ 3NaBrO4+Xe
 查看习题详情和答案>>
查看习题详情和答案>>
(1)铅(原子序数为82)从单质到其化合物都有着广泛的应用,如制造焊锡、铅蓄电池、化工耐酸设备以及X射线的防护材料等.铅的氧化物主要有三种:PbO、PbO2和Pb3O4.请回答下列问题:
①铅位于元素周期表中第______周期第______族;
②PbO2是一种两性氧化物,试写出PbO2和NaOH浓溶液反应的离子方程式:______.
(2)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图______.
(3)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑.请预测首先被用来与F2反应制备稀有气体化合物的元素是______(填写字母).利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式______ 3NaBrO4+Xe
 查看习题详情和答案>>
查看习题详情和答案>>